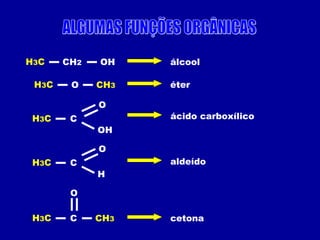
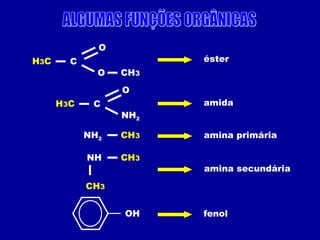
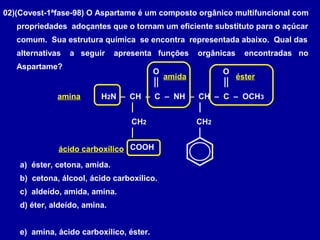
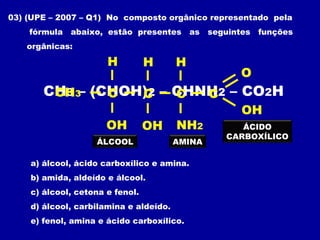
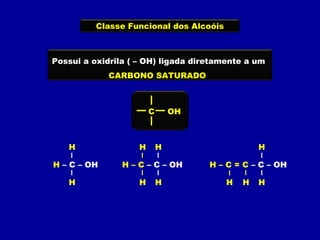
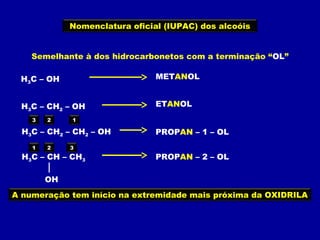
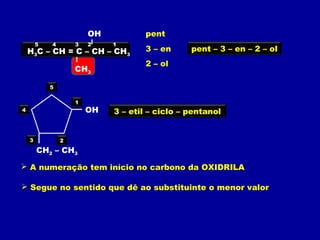
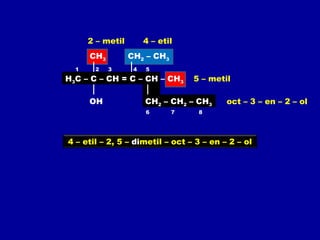
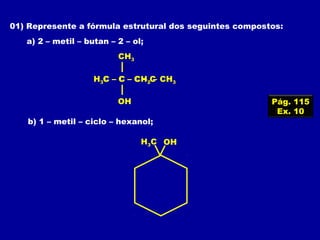
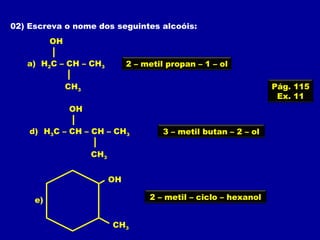
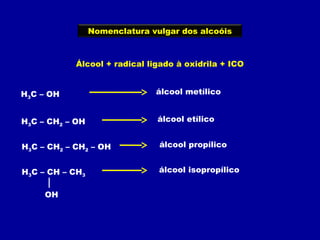
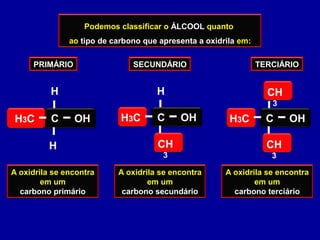
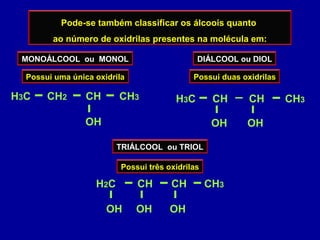
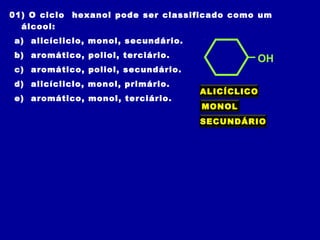
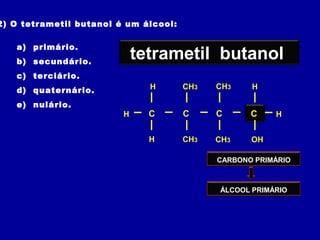
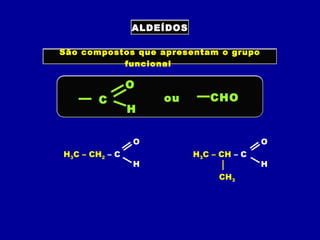
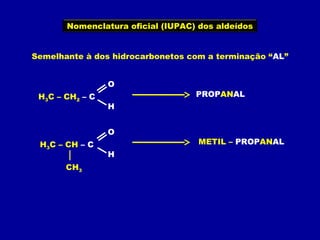
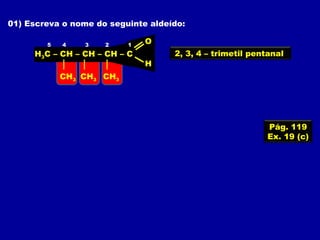
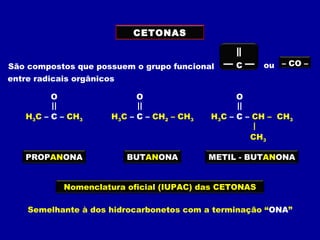
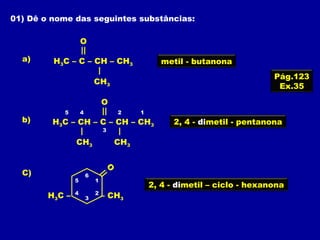
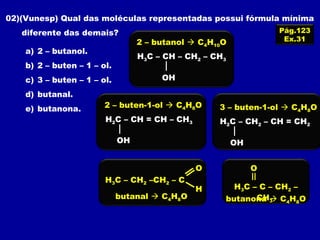
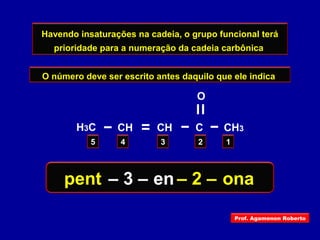
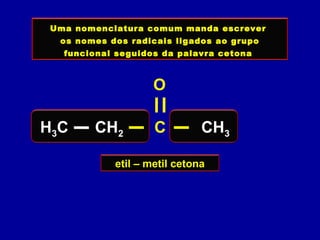
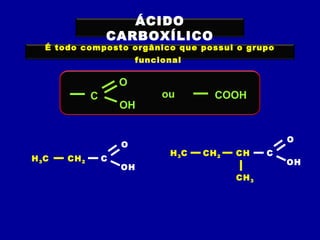
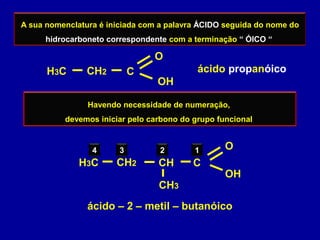
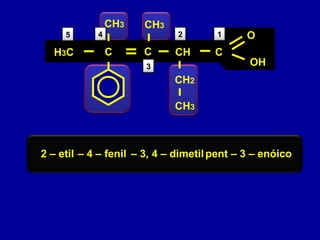
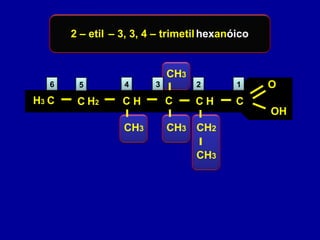
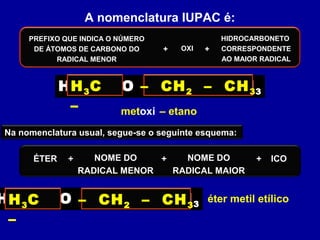
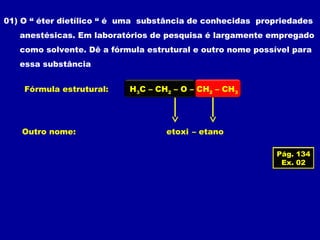
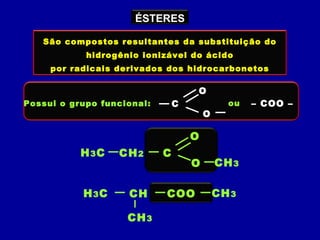
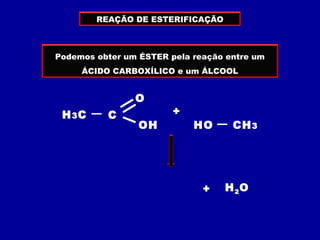
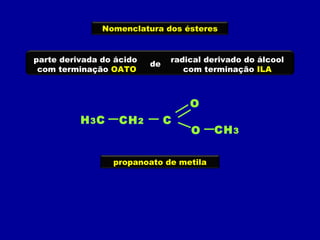
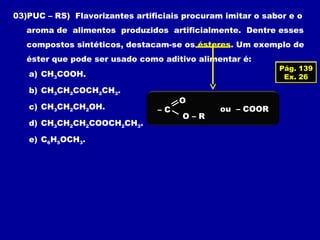
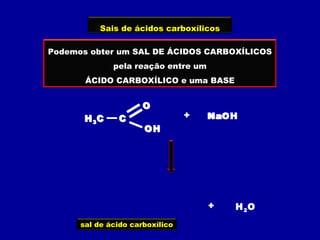
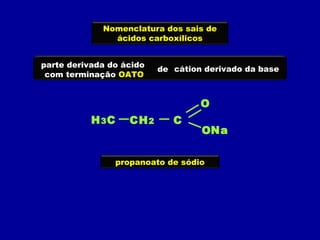
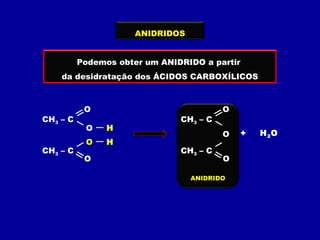
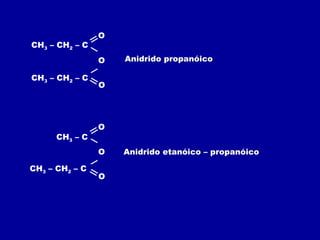
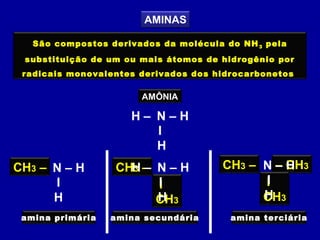
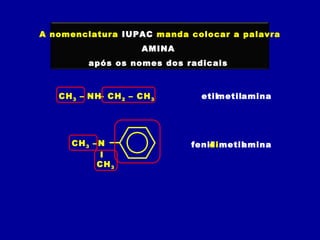
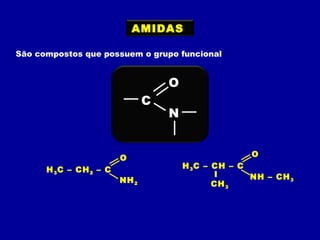
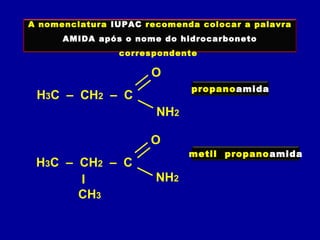
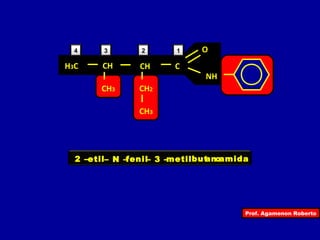
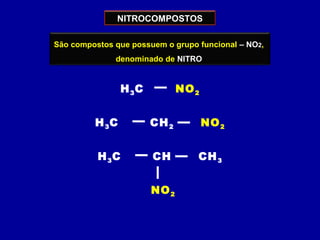
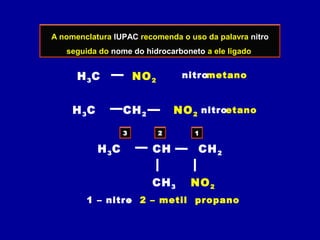
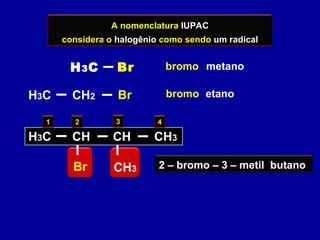
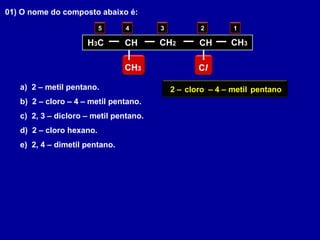
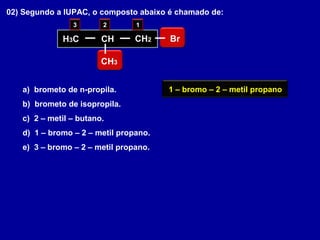
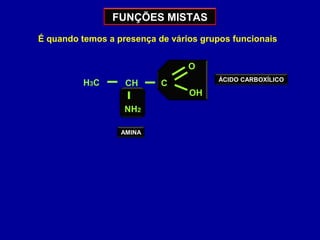
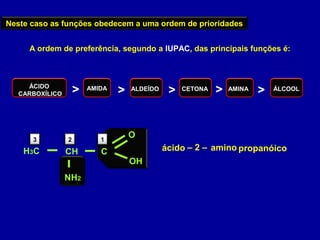
O documento descreve as principais classes de compostos orgânicos identificadas por seus grupos funcionais característicos. São eles: álcoois, identificados pelo grupo hidroxila -OH; aldeídos, identificados pelo grupo carbonila CHO; e cetonas, identificados pelo grupo carbonila CO. A nomenclatura destes compostos segue regras similares aos hidrocarbonetos com terminações específicas para cada função.