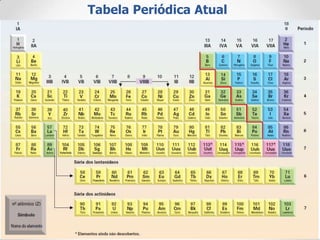
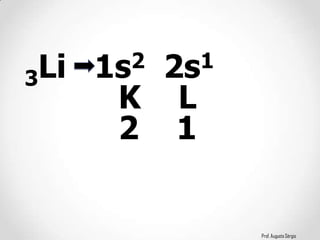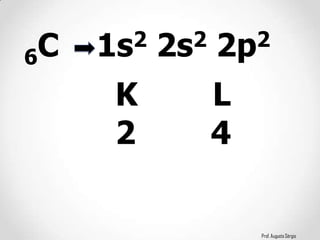O documento descreve uma aula sobre a Tabela Periódica dos Elementos Químicos, abordando seus principais conceitos como:
1) A origem e objetivos da Tabela Periódica;
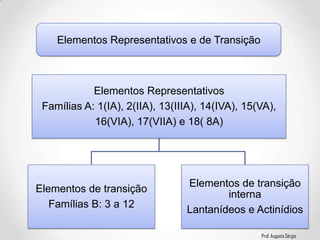
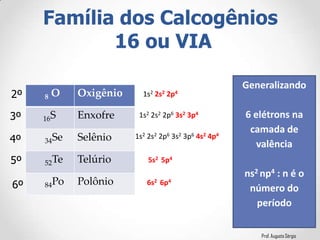
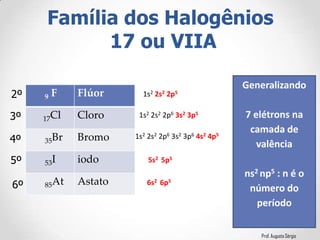
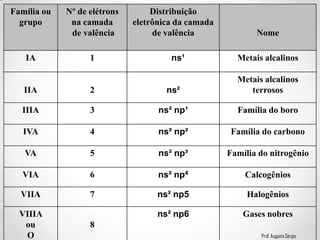
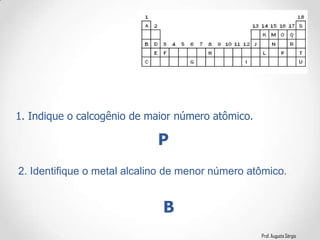
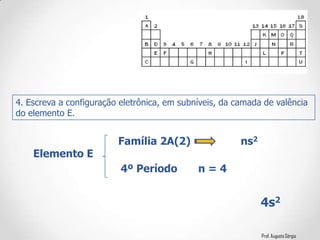
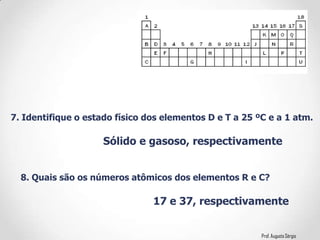
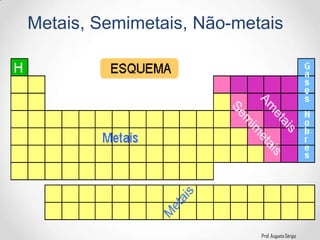
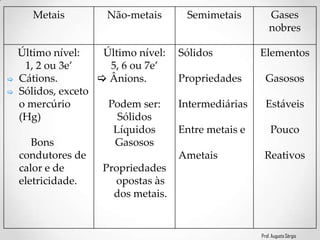
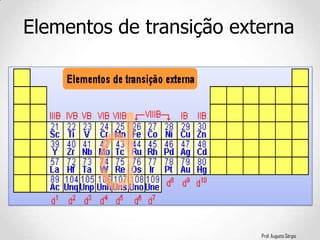
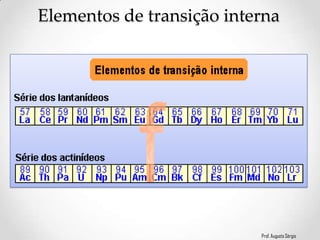
2) A classificação dos elementos de acordo com suas propriedades e posição na Tabela;
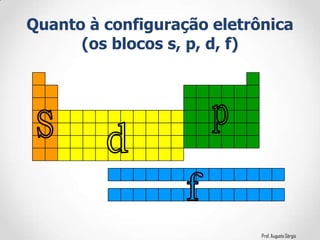
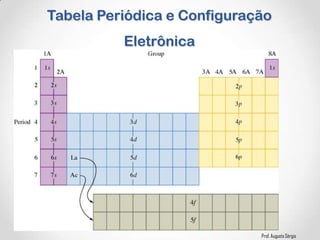
3) A relação entre a configuração eletrônica e a posição dos elementos nos diferentes grupos.