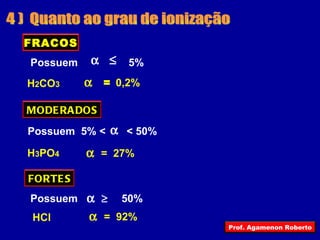
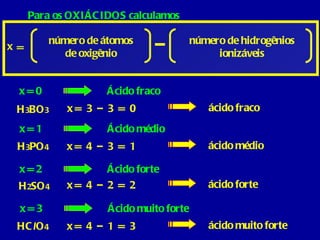
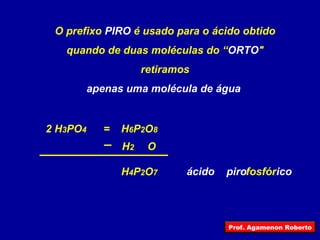
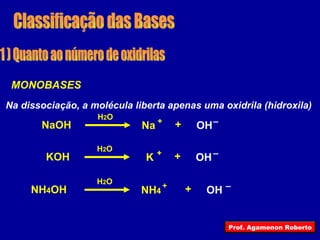
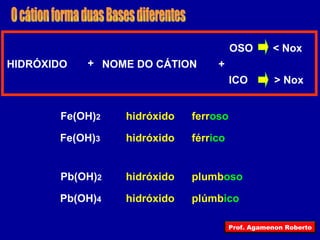
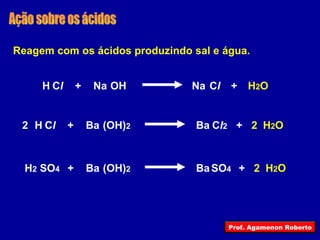
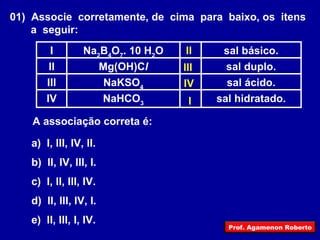
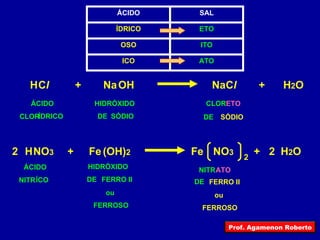
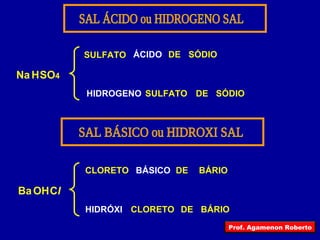
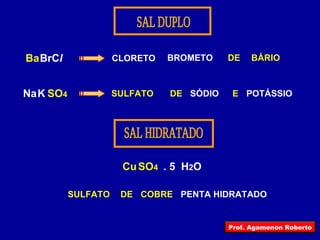
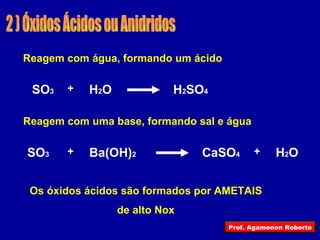
O documento descreve as principais funções inorgânicas, incluindo ácidos, bases e sais. Explica a ionização e dissociação e como isso diferencia ácidos de bases. Detalha a classificação de ácidos e bases de acordo com suas propriedades, como número de hidrogênios ionizáveis, presença de oxigênio, número de elementos químicos e grau de ionização.












![2 ) Quanto à presença do oxigênio HIDRÁCIDOS OXIÁCIDOS HCl HCN H 2 S H 4 [Fe(CN) 6 ] São ácidos que não possuem o elemento químico OXIGÊNIO HNO 3 H 2 CO 3 H 2 SO 4 H 3 PO 4 São ácidos que possuem o elemento químico OXIGÊNIO Prof. Agamenon Roberto](https://image.slidesharecdn.com/funcaoinorganica3-110921175049-phpapp01/85/Funcao-inorganica3-17-320.jpg)
![3 ) Quanto ao número de elementos químicos HCl H 4 [Fe(CN) 6 ] H 2 CO 3 HCN H 2 SO 4 H 2 S Possuem apenas dois elementos químicos BINÁRIOS Possuem apenas três elementos químicos TERNÁRIOS Possuem apenas quatro elementos químicos QUATERNÁRIOS Prof. Agamenon Roberto](https://image.slidesharecdn.com/funcaoinorganica3-110921175049-phpapp01/85/Funcao-inorganica3-18-320.jpg)