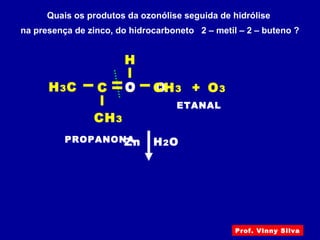
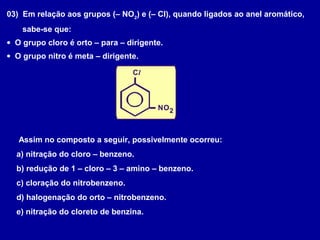
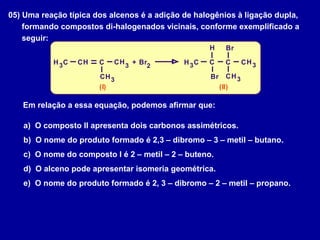
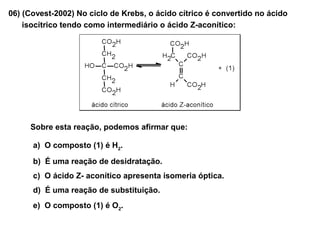
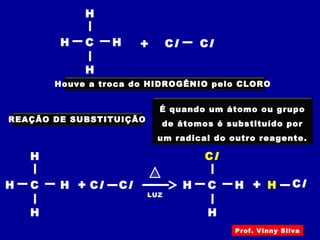
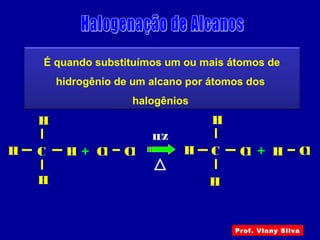
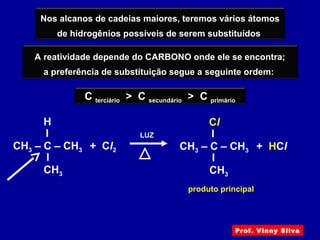
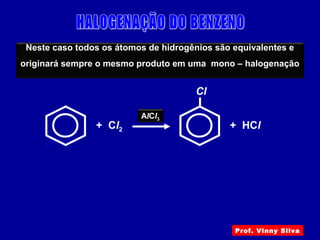
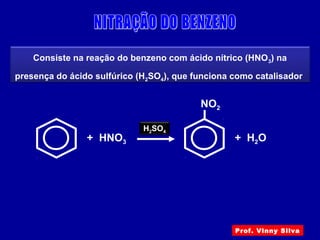
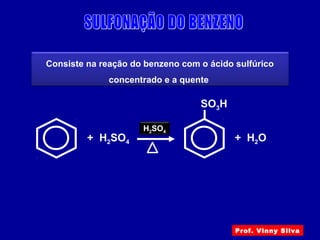
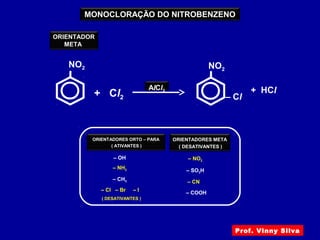
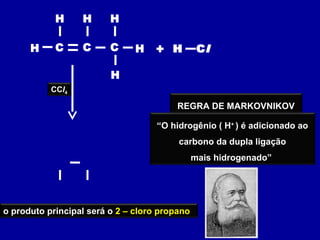
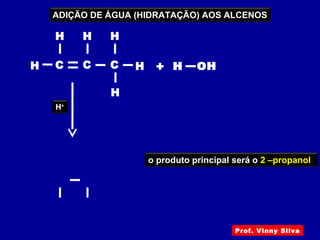
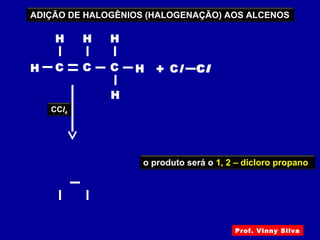
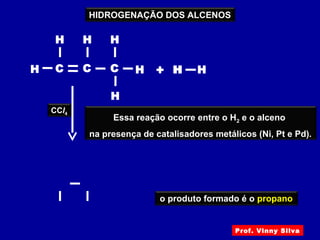
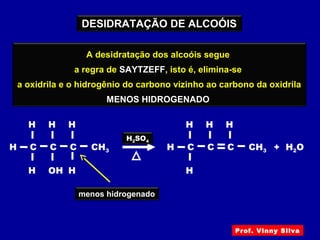
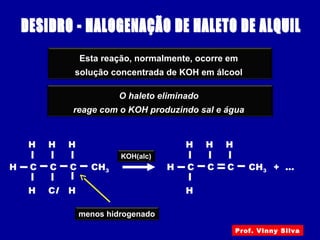
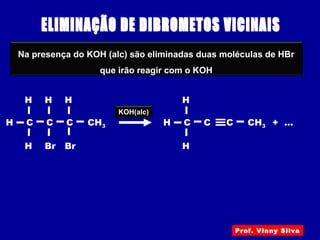
O documento descreve diferentes tipos de reações orgânicas como substituição, adição e eliminação. A reação de substituição envolve a troca de átomos ou grupos. A reação de adição envolve a formação de uma nova ligação molecular. A reação de eliminação envolve a remoção de átomos ou grupos sem substituição.














![OXIDAÇÃO DE ALCOÓIS
O comportamento dos alcoóis primários, secundários e terciários,
com os oxidantes, são semelhantes
Os alcoóis primários, sofrem oxidação, produzindo aldeído
H3C
ETANOL
– C
I
I
– OH
H
H
[O]
H3C – C
H
O
ETANAL– H2O
O aldeído, se deixado em contato com o
oxidante, produzácido
carboxílico.
H3C – C
H
O
ETANAL
[O]
H3C – C
OH
O
ÁCIDO ETANÓICO
– H2O](https://image.slidesharecdn.com/reaesorganicas-vinny-150722212816-lva1-app6891/85/Reacoes-Organicas-32-320.jpg)
![Os alcoóis secundários oxidam-se formando cetonas.
H3C –
2 – PROPANOL
C
I
I
– CH3
OH
H
[O]
H3C – C
II
– CH3
– H2O
O
PROPANONA
Obs.: Os alcoóis terciários não sofrem oxidação
Prof. Vinny Silva](https://image.slidesharecdn.com/reaesorganicas-vinny-150722212816-lva1-app6891/85/Reacoes-Organicas-33-320.jpg)
![OXIDAÇÃO DE ALCENOS
Os alcenos sofrem oxidação branda originando dialcoóis vicinais
H3C – C
I
I
– CH3
OH
H
[O]
= C
I
H
branda
H3C – C
I
– CH3
H
– C
I
H
I
OH
Prof. Vinny Silva](https://image.slidesharecdn.com/reaesorganicas-vinny-150722212816-lva1-app6891/85/Reacoes-Organicas-34-320.jpg)
![A oxidação a fundo, com quebra da ligação dupla, produz
ácido carboxílico e /ou cetona
H3C – C
I
– CH3
H
[O]
= C
I
H
a fundo
H3C – C
I
H
= O + – CH3= C
I
H
OH3C – C
OH
O
2
Prof. Vinny Silva](https://image.slidesharecdn.com/reaesorganicas-vinny-150722212816-lva1-app6891/85/Reacoes-Organicas-35-320.jpg)