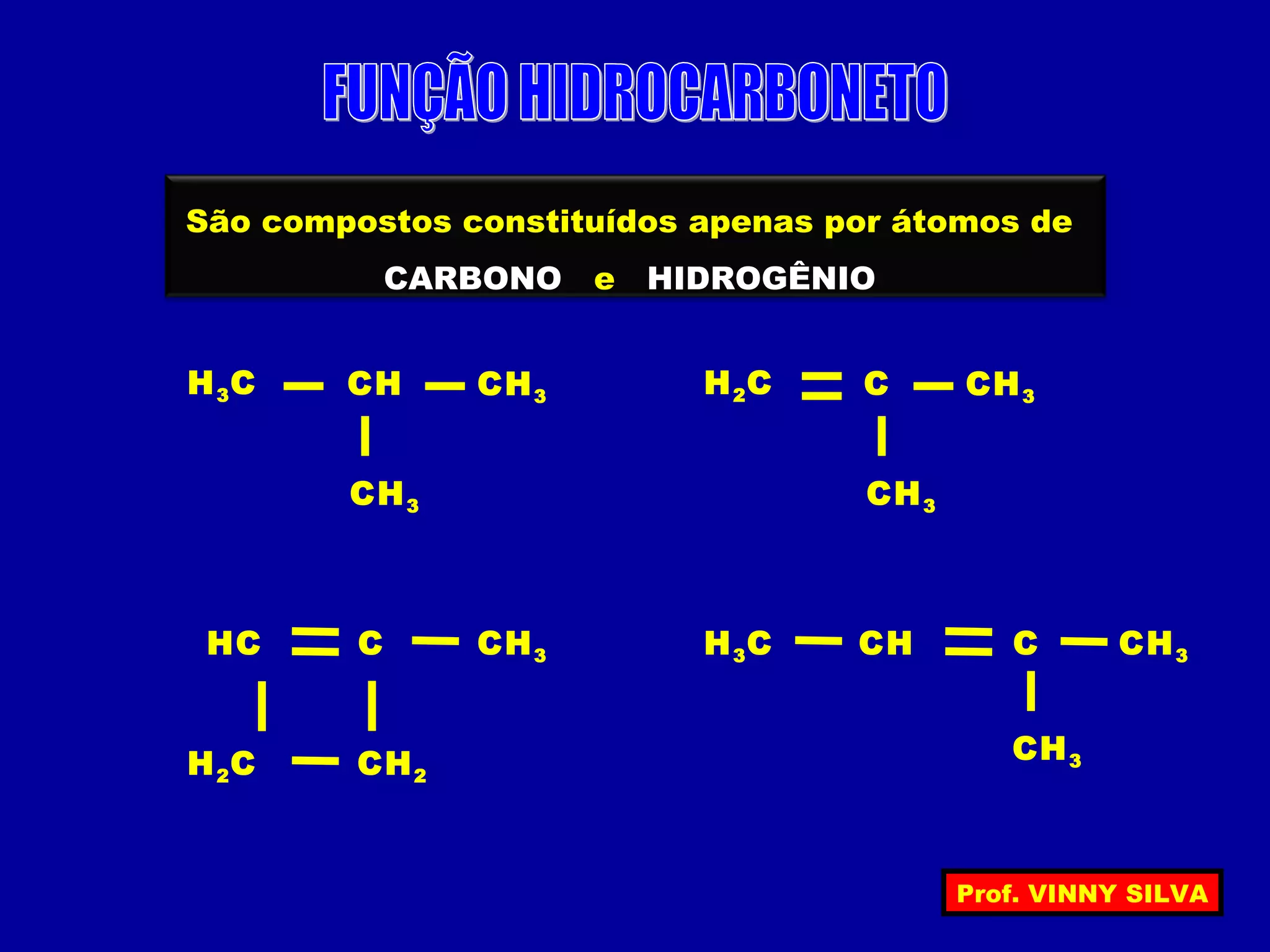
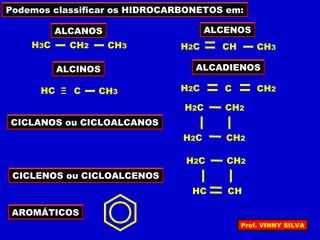
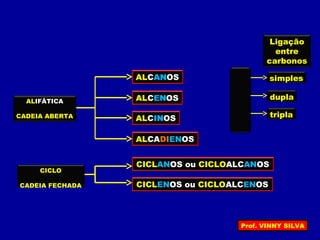
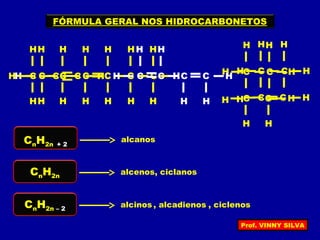
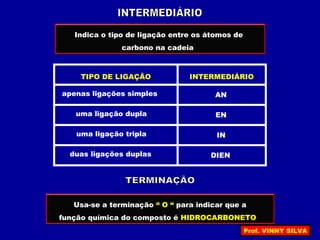
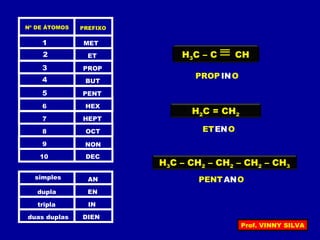
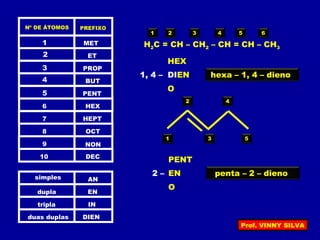
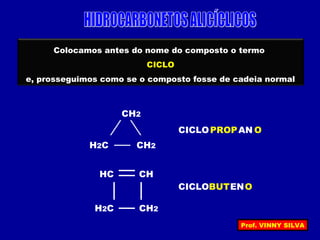
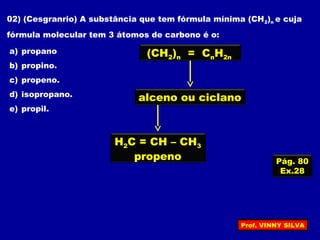
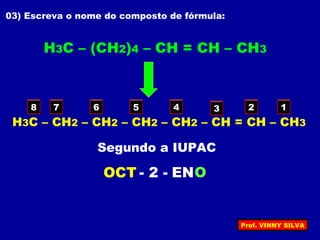
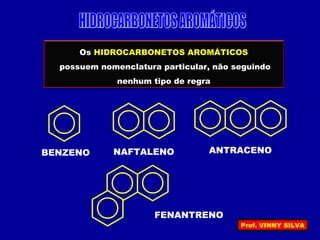
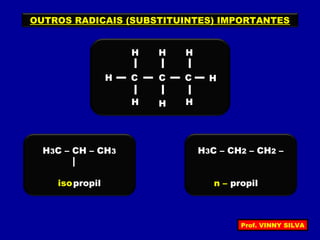
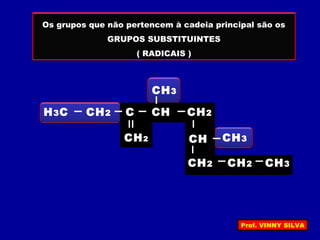
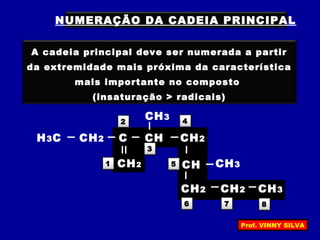
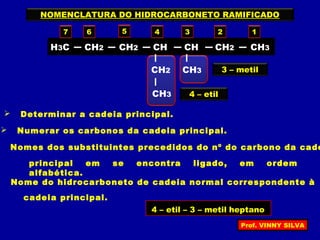
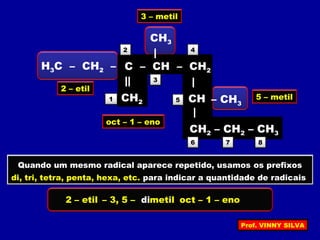
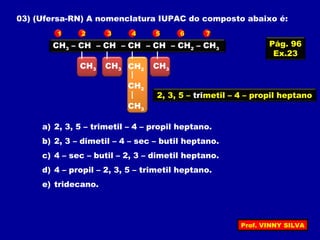
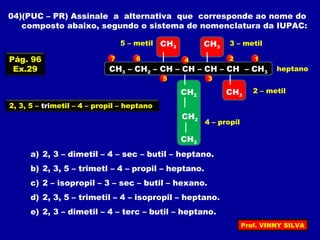
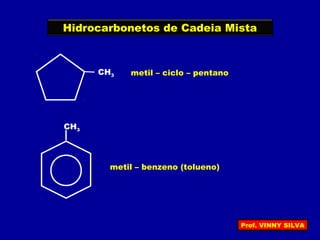
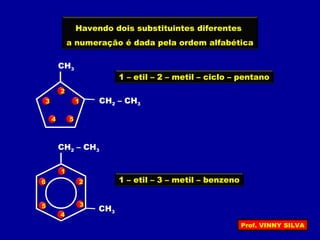
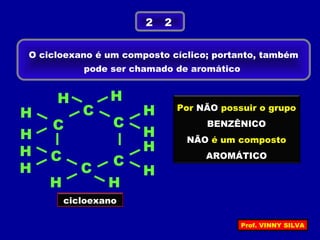
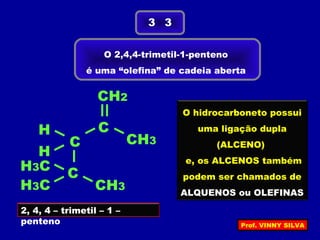
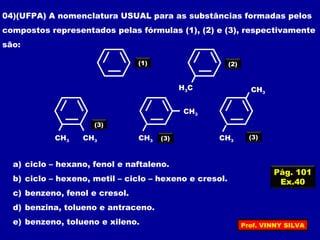
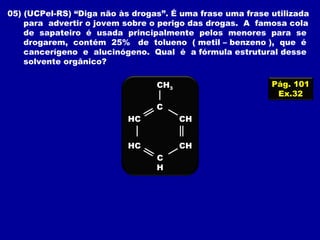
[I] Os hidrocarbonetos são compostos formados apenas por carbono e hidrogênio. [II] Eles podem ser classificados em alcanos, alcenos e alcinos de acordo com o tipo de ligação entre os carbonos. [III] A nomenclatura IUPAC fornece regras para nomear esses compostos de forma sistemática indicando o número de átomos de carbono, tipo de ligação e posição de insaturações.