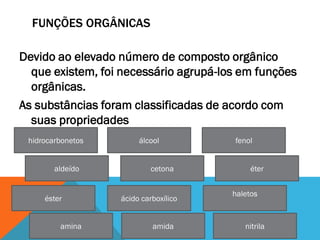
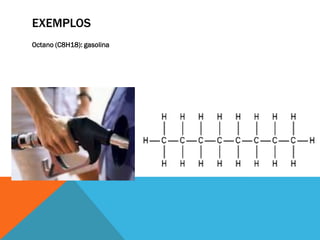
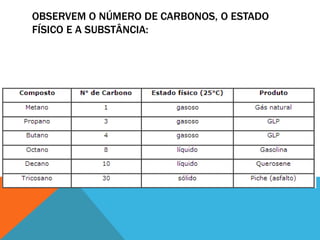
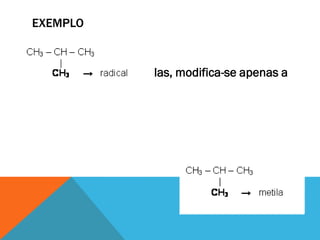
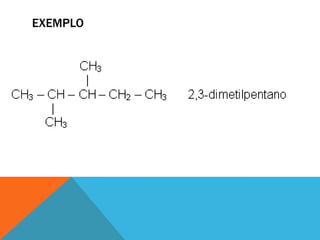
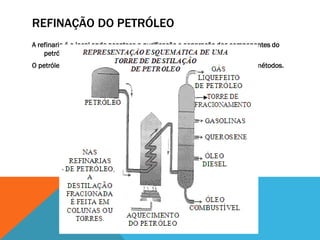
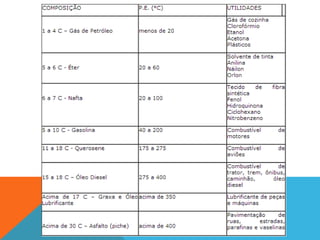
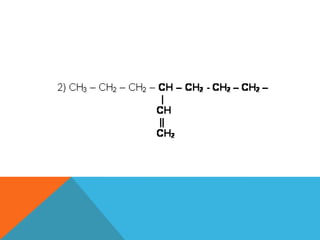
Este documento descreve as principais funções orgânicas e subclasses de hidrocarbonetos. Apresenta definições, exemplos e aplicações dos alcanos, alcenos, alcadienos e alcinos. Explica a classificação, nomenclatura e propriedades destes compostos, com ênfase na importância dos hidrocarbonetos derivados do petróleo para a indústria química e de combustíveis.