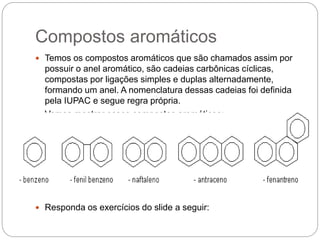
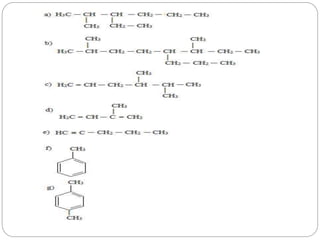
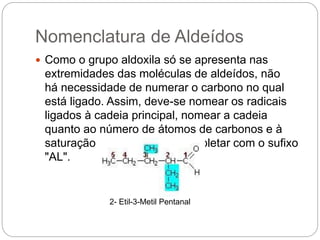
O documento apresenta uma introdução às funções orgânicas, dividindo-as em hidrocarbonetos, álcoois e aldeídos. Explica que as funções orgânicas contêm carbono ligado a hidrogênio e outros elementos, e que o carbono possui capacidade de ligar-se a quatro elementos. Detalha a nomenclatura e classificação dos principais tipos de compostos orgânicos.