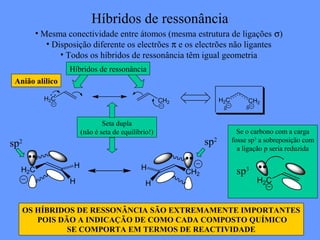
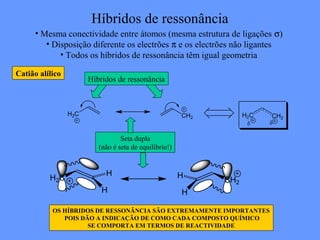
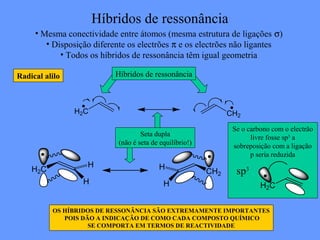
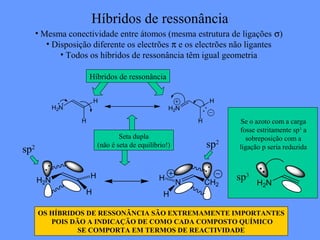
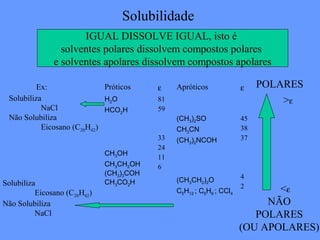
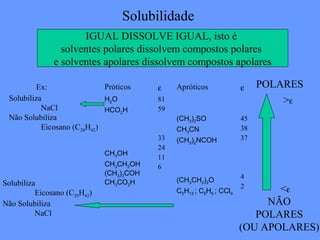
O documento discute a solubilidade de compostos em solventes polares e apolares. Explica que compostos polares se dissolvem em solventes polares com alto valor de constante dielétrica, enquanto compostos apolares se dissolvem em solventes apolares com baixo valor de constante dielétrica. Fornece exemplos como água, etanol e acetona como solventes polares, e hexano, benzeno e tetraclorometano como solventes apolares.