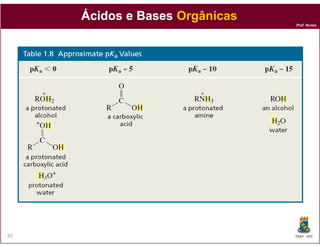
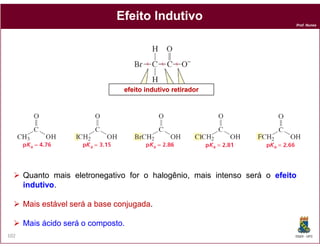
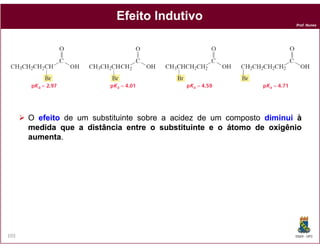
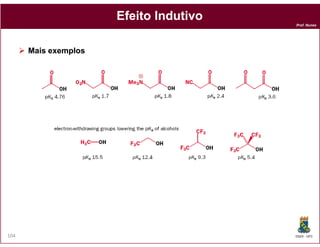
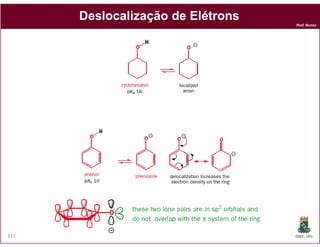
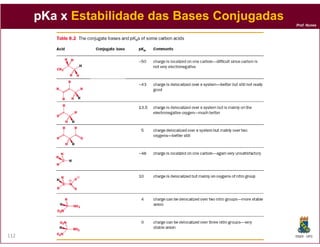
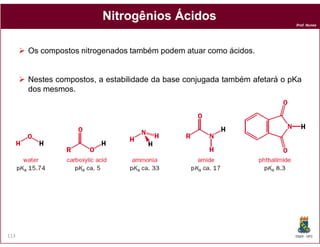
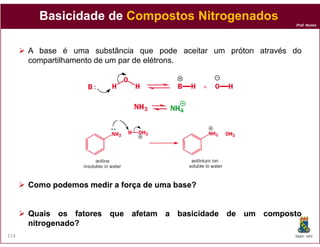
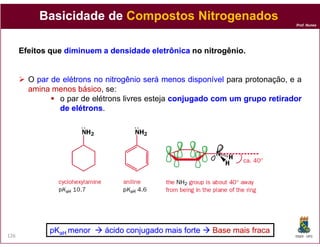
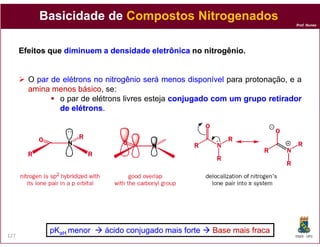
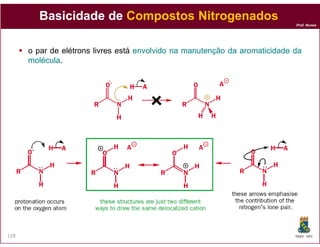
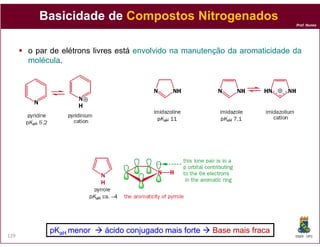
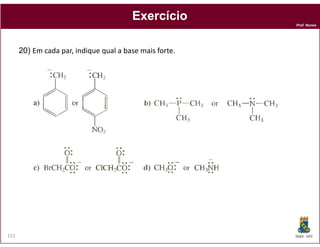
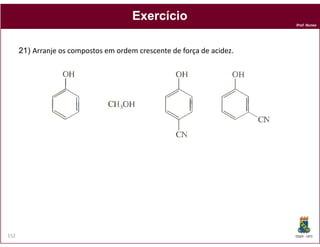
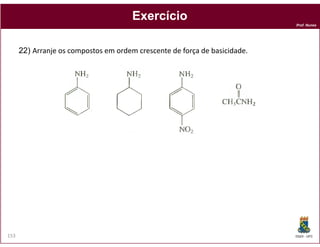
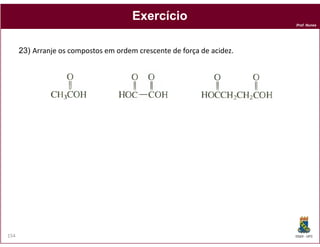
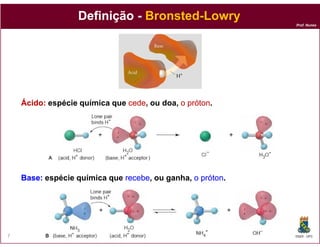
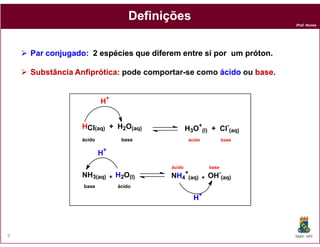
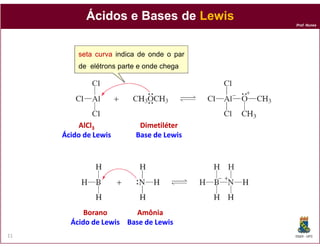
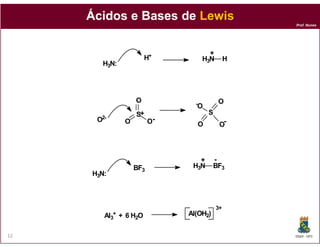
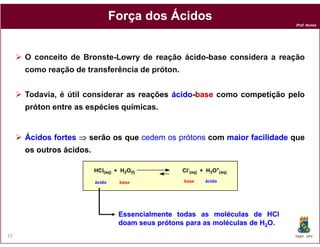
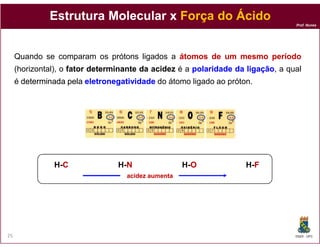
O documento discute os conceitos fundamentais de ácidos e bases, incluindo as definições de Arrhenius, Bronsted-Lowry e Lewis. Também aborda tópicos como a força relativa de ácidos, constantes de acidez e basicidade, autoionização da água, escala pH e cálculos envolvendo concentrações iônicas em soluções aquosas.










![Constantes de Acidez
Prof. Nunes
Todas estas espécies estão em equilíbrio dinâmico.
dinâmico
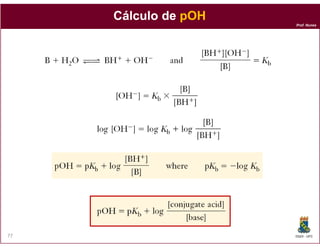
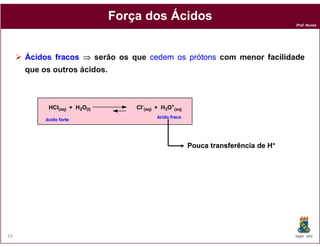
Como os ácidos e bases conjugados estão em equilíbrio na solução,
podemos expressar a composição da solução de um ácido ou base
em termos da constante de equilíbrio para a transferência de prótons.
CH3COOH + H2O H3O+ + CH3COO-
Ka = [H3O+] [CH3COO-]
[CH3COOH]
Ka = 1,8 x 10-5 (25oC)
19 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-19-320.jpg)








![Calculando a [H3O+] a partir do pH
Prof. Nunes
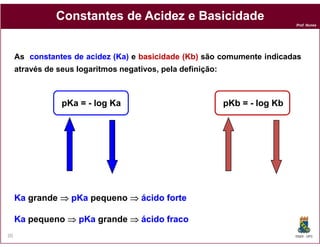
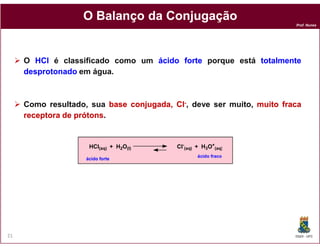
O pH de uma solução é 3,301. Qual é a concentração de H3O+ nesta solução?
32 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-32-320.jpg)


![Relações entre [H3O+], pH, pOH, e [OH-]
pOH,
Prof. Nunes
35 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-35-320.jpg)
![Cálculos Envolvendo pH e pOH
Prof. Nunes
Calcule a [H3O+], pH, [OH-], pOH para uma solução 0,015 M de HNO3.
36 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-36-320.jpg)
![Cálculos Envolvendo pH e pOH
Prof. Nunes
Calcule a [H3O+], pH, [OH-], pOH para uma solução 0.015 M Ca(OH)2.
37 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-37-320.jpg)




![Cálculos de Ka e Pka
Prof. Nunes
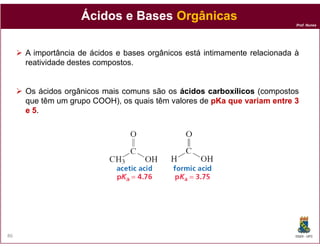
O ácido nicotínico é um ácido orgânico fraco
monoprótico que podemos representar como HA.
HA
Uma solução diluída de ácido nicotínico contém as seguintes concentrações
em equilíbrio a 25 ° C. [HA] = 0,049 M; [H3O+] = [A-] = 8,4 10-4 M. Determine o
valor de Ka?
43 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-43-320.jpg)



![Exercício
Prof. Nunes
O ácido nicotínico (HNIc) é um ácido fraco monoprótico. Uma solução 0,012M
tem pH = 3,39 a 25 oC. Qual a constante Ka e o grau de ionização?
Concentração HNic H+ + Nic-
início 0,012 ~0 0
variação -x +x +x
equilíbrio 0,012 - x x x
Ka = [H3O+] [Nic-] = x2 = (0,00041)2 = 1,4 x 10-5
0,012
[HNic] (0,012 - x)
x = [H+] = 10-pH = 10-3,39 = 0,00041
47 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-47-320.jpg)
![Exercício
Prof. Nunes
O ácido nicotínico (HNIc) é um ácido fraco monoprótico. Uma solução 0,012M
tem pH = 3,39 a 25 oC. Qual a constante Ka e o grau de ionização?
Concentração HNic H+ + Nic-
início 0,012 ~0 0
variação -x +x +x
equilíbrio 0,012 - x x x
Ka = [H3O+] [Nic-] = x2 = (0,00041)2 = 1,4 x 10-5
[HNic] (0,012 - x) 0,012
Grau de ionização = x * 100 = 3,4%
0,012
48 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-48-320.jpg)

![Exercício
Prof. Nunes
Concentração HNic H+ Nic-
+
início 0,10 ~0 0
variação -x +x +x
equilíbrio 0,10 - x x x
Ka = [H3O+] [Nic-] = x2 = 1,4 x 10-5
[Hnic] (0,10 - x)
Simplificando.... se Ka é muito pequeno [H+] é muito pequena
logo (0,10 – x) = 0,10
Ka = x2 x = 0,0012
0,10
50 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-50-320.jpg)
![Exercício
Prof. Nunes
+
x= [H+] = 0,0012 pH = - log 0,0012 = 2,92
Grau de ionização = x = 0,0012 * 100 = 1,2%
0,10 0,10
51 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-51-320.jpg)
![Hipótese Simplificadora
Prof. Nunes
Sempre poderemos usar a hipótese simplificadora
simplificadora?
Pode-se mostrar que o erro introduzido pela hipótese simplificadora é
menor que 5% se: concentração do ácido ≥ 100
Ka
Exemplo 1) [HA] = 10-2 = 103 hipótese aceitável
Ka = 10-5
Exemplo 2) [HA] = 10-4 = 10 hipótese não-aceitável
não-
Ka = 10-5 (Resolver equação do 2o grau)
52 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-52-320.jpg)






![Cálculos das Concentrações
Prof. Nunes
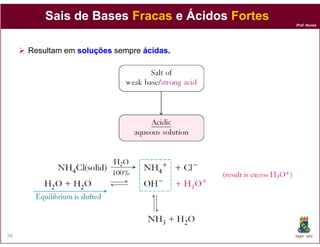
Qual o pH do nicotinato de sódio 0,10 M (Ka = 1,4 x 10-5).
Nic-(aq) + H2O(l) HNic(aq) + OH-(aq)
Kb = Kw = 10-14 = 7,1 x 10-10
Ka 1,4 x 10-5
Kb = [HNic] [OH-] = x2 = 7,1 x 10-10
[Nic-] 0,10 – x
x = [OH-] = 8,4 x 10-6 pOH = 5,08
pH = 8, 92 (alcalino)
63 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-63-320.jpg)

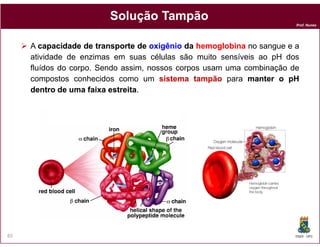



![Solução Tampão: Ácido Fraco + Sal
Tampão:
Prof. Nunes
(completo)
(reversível)
Ambos CH3COOH e CH3COO- Na+ são fontes de íons CH3COO-.
O CH3COO- Na+ completamente dissociado fornece uma alta [CH3COO- ].
CH
Isso altera o equilíbrio de ionização do CH3COOH para a esquerda através
da combinação dele com H3O+ para formar CH3COOH não-ionizado e H2O.
O resultado é uma diminuição drástica da [H3O+] na solução.
Soluções que contêm um ácido fraco mais um sal do ácido fraco são
sempre menos ácidas que as soluções que contêm a mesma
concentração do ácido fraco sozinho.
sozinho.
69 DQOI - UFC](https://image.slidesharecdn.com/acidosebases-111101133643-phpapp02/85/Acidos-e-Bases-69-320.jpg)