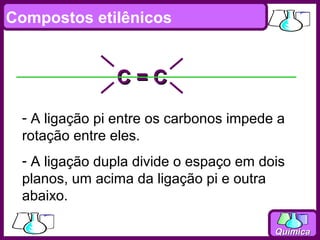
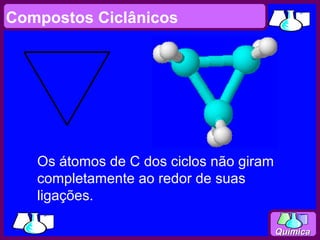
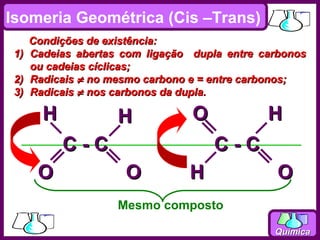
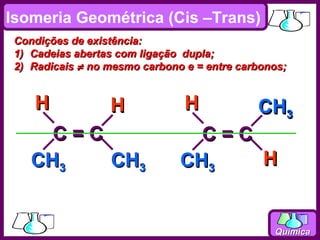
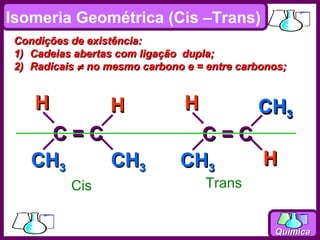
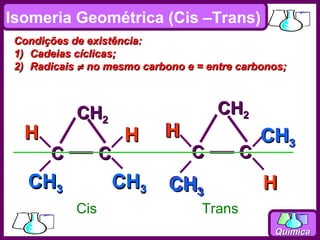
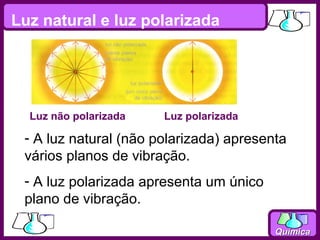
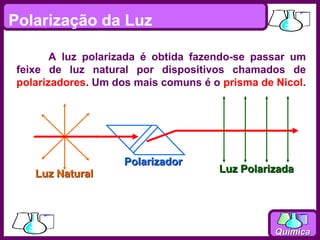
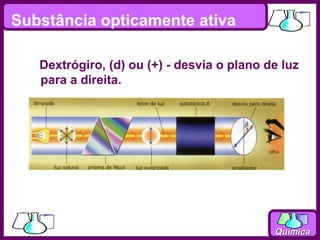
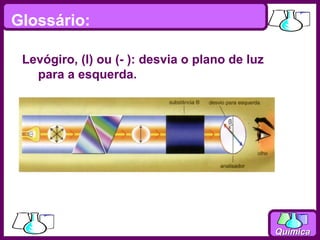
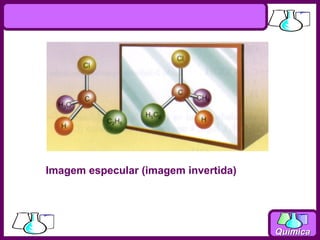
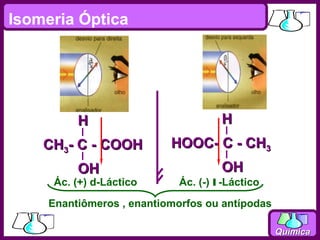
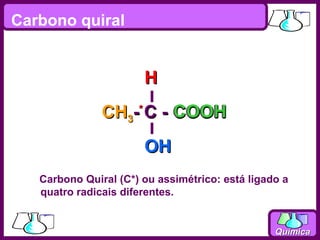
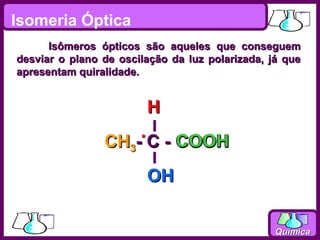
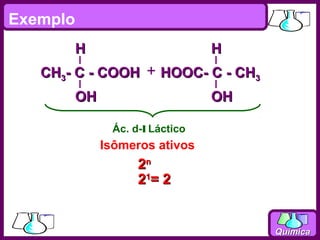
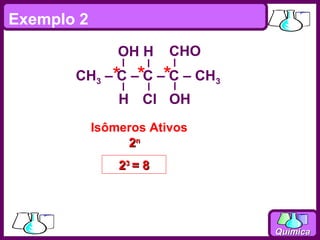
O documento discute isomeria espacial, classificando estereoisômeros em diastereoisômeros e enantiômeros. Também aborda isomeria geométrica em compostos etilênicos e ciclânicos, definindo isômeros cis e trans. Por fim, explica isomeria óptica, definindo substâncias opticamente ativas e inativas, e discutindo carbonos quirais e o número de isômeros ópticos possíveis.