Este documento discute compostos de coordenação, incluindo sua estrutura, ligantes e números de coordenação. Compostos de coordenação são formados por um íon metálico ligado a ligantes por ligações coordenadas. O documento descreve os tipos de ligantes, como monodentado, bidentado e quelato, e discute a teoria dos compostos de coordenação desenvolvida por Alfred Werner no século 19.

![O que é um composto de coordenação?
Compostos formados por um íon metálico de transição (na maioria dos
casos) envolvido por átomos, moléculas ou grupos de átomos (ligantes).
Para que um ligante possa participar de um
complexo é fundamental que o mesmo
contenha pares eletrônicos disponíveis para
carga do
complexo
efetuar ligações coordenadas.
Um complexo pode ser catiônico, aniônico
ou neutro.
Neutros: [Ni(CO)4]
Iônicos: [Fe(CN)6]K4, [Cu(H2O)4]SO4
X+/-
n
n+/-
ligantes
íon metálico
contraíon](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-2-320.jpg)
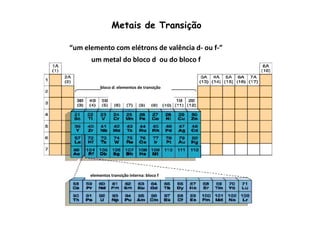
![Distribuição eletrônica nos átomos dos metais de transição
Sc
Ti
V
Cr
3d 4s 4p
[Ar]3d14s2
[Ar]3d24s2
[Ar]3d34s2
[Ar]3d54s1 Mn
Fe
Co
Ni
Cu
Zn
3d 4s
[Ar]3d54s2
[Ar]3d64s2
[Ar]3d74s2
[Ar]3d84s2
[Ar]3d104s1
[Ar]3d104s2](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-4-320.jpg)
![Números de elétrons d
[Ar]3d54s2 [Ar]3d104s1
1º. Quantos elétrons estão contidos nos metais d?
- Contagem na tabela períódica Mn = 7 elétrons Cu = 11 elétrons
2º. Quantos elétrons foram perdidos? - estado de oxidação
Mn (VII) = 7 elétrons perdidos Cu(II) = 2 elétrons perdidos
3º. Quantos elétrons sobram? - subtração
Mn (VII) = 7-7 = zero elétrons d = d0 Cu(II) = 11-2 = 9 elétrons d = d9
RReeggrraa: Os elétrons s são os primeiros a serem perdidos
elétrons de valência em um metal de transição = elétrons d](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-5-320.jpg)
![Exercício: Quantos elétrons d tem o metal?
complexo Nox de L Nox do M nº elétrons d
[Cr2O7]2- - 2 +6 d0
[[MMnnOO4]]-- -- 22 ++77 dd00
[Ag(NH3)2]+ 0 +1 d10
[Ti(H2O)6]3+ 0 +3 d1
[Co(en)3]3+ 0 +3 d6
[PtCl2(NH3)2] - 1, 0 +2 d8
[V(CN)6]4- - 1 +2 d3
[Fe(ox)3]3- - 2 +3 d5
NHH 2 2N
O O
-O O-ox
en =
=](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-6-320.jpg)
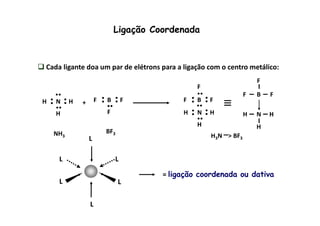
![Sidwick 1927 - modelo de ligação
Exemplo: [Co(NH3)6]3+
“base de Lewis
NH3
3+
6 + Co3+
H
N
H
H
H3N
“ácido de Lewis
NH3
NH3
H3N
NH3](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-8-320.jpg)
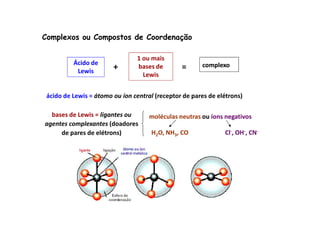

![Teoria de Werner (1893)
1. O metal está em um estado de oxidação particular (valência primária)
2. O composto tem um número de coordenação (valência secundária).
3. Os ligantes estão coordenados ao metal via uma ligação que parece com
uma ligação covalente.
[Co(NH3)6]Cl3
3+
[Co(NH3)5Cl]Cl2
2+
[Co(NH3)4Cl2]Cl
+
[Co(NH3)3Cl3]
3 moles AgCl 2 moles AgCl 1 mol AgCl 0 mol AgCl](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-11-320.jpg)
![Fórmula Empírica
Medidas de condutividade
Condutividade (C = 0,001
mol/L)
Formulação de Werner
Não Eletrólitos
PtCl4.2NH3 3,52 [Pt(NH3)2Cl4] (trans)
PtCl4.2NH3 6,99 [Pt(NH3)2Cl4] (cis)
Eletrólitos 1:1
NaCl 123,7 -------
PtCl4.3NH3 96,8 [Pt(NH3)3Cl3]Cl
PtCl4.NH3.KCl 106,8 K[Pt(NH3)Cl5]
Eletrólitos 1:2 ou 2:1
CaCl2 260,8 -------
CoCl3.5NH3 261,3 [Co(NH3)5Cl]Cl2
CoBr3.5NH3 257,6 [Co(NH3)5Br]Br2
CrCl3.5NH3 260,2 [Cr(NH3)5Cl]Cl2
PtCl4.4NH3 228,9 [Pt(NH3)4Cl2]Cl2
PtCl4.2KCl 256,8 K2[PtCl6]
Eletrólitos 1:3 ou 3:1
LaCl3 393,5 -------
CoCl3.6NH3 431,6 [Co(NH3)6]Cl3
CrCl3.6NH3 441,7 [Cr(NH3)6]Cl3
PtCl4.5NH3 404,0 [Pt(NH3)5Cl]Cl3](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-12-320.jpg)
![Teoria de Werner
Explicação para a ligação nos complexos baseada nos ensaios:
Medidas de condutividade
[Cr(H2O)6]3+ 3Cl- [Cr(H2O)5Cl]2+ 2Cl- [Cr(H2O)4Cl2]+ Cl-
Existência de 2 tipos de valência:
1) valência primária (dissociável)
2) valência secundária (não dissociável)
Ligações iônicas
cátion complexo – ânion
Ligação coordenativa
ligante – átomo ou íon metálico](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-13-320.jpg)
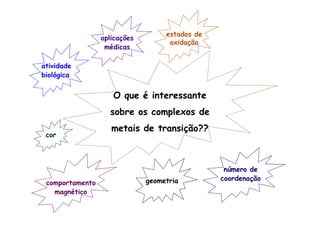

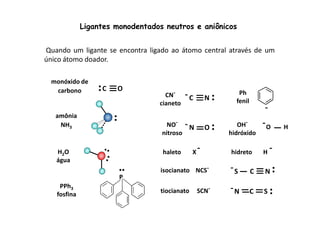
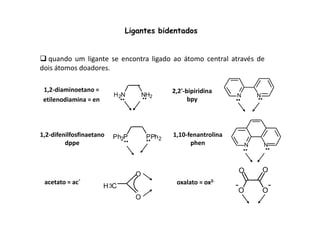
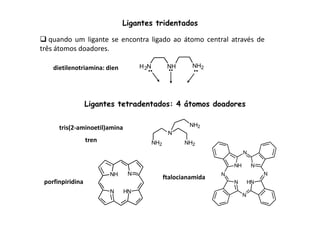
![Ligantes multidentados
tetraânion do ácido etilenodiaminatetraacético: EDTA
- N N
-
O
O
-
O
-
O
O O
O
O O
Hexadentado
O
O N
M
O N
O
O
O
O
[Co(EDTA)]-](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-19-320.jpg)
![Os ligantes que estão diretamente ligados ao átomo ou íon central
formam um complexo de esfera interna.
No entanto, os íons complexos podem associar-se
eletrostaticamente a ligantes aniônicos, sem o deslocamento dos
ligantes já presentes. O produto desta associação é chamado de
complexo de esfera externa ou par iônico.
Os complexos nos quais um metal se encontra lliiggaaddoo aa uumm úúnniiccoo
tipo de grupo doador (ligante) são conhecidos como complexos
homolépticos. Ex.: [Co(NH3)6]+3
Os complexos nos quais um metal se encontra ligado a mais de um
tipo de ligante são conhecidos como complexos heterolépticos. Ex.:
[Co(NH3)4Cl2]+](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-20-320.jpg)
![número de coordenação = o número de ligantes que envolvem o átomo do
metal.
Por exemplo: no complexo
[Co(NH3)6]Cl3, o número de
NH3
3+
Número de Coordenação
coordenação é 6, pois existem 6
moléculas de amônia ligadas ao íon
cobalto(III).
Os ligantes representados fora dos
colchetes (Cl-) não fazem parte do
número de coordenação.
H3N
CCoo
NH3
NH3
H3N
NH3
3 Cl-](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-21-320.jpg)

![Número de coordenação 2
Os complexos com NC=2 são lineares e praticamente se restringem
aos cátions: Cu+, Ag+, Au+ e Hg+2, todos com configuração d10.
Ex.: [CuCl2]-; [Ag(NH3)2]+; [AuCl2]- e HgCl2.
[Au(CN)2]-
180º
[AgCl2]-
180º
[CuCl2]-
180o](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-23-320.jpg)
![Número de coordenação 3
a coordenação tripla é rara entre os complexos metálicos. Aparece
normalmente em complexos com ligantes volumosos, como o amideto
[N(Si(CH3)3)2]-. Estes complexos exibem geometria trigonal planar.
Ex.: M{[N(Si(CH3)3)2]-}3, M= Fe, Cr
CN
CN
[HgI3]-
120o
[Cu(CN)2]- Cu
C
N
Cu
CN
C
N
Cu
C
N
Cu
CN
C
N
n](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-24-320.jpg)
![Número de coordenação 4
Este tipo de coordenação é encontrada em um grande número de
compostos e podem apresentar geometria tetraédrica ou quadrática.
Os complexos com geometria tetraédrica ocorrem com metais que não
possuam configuração d8 (ou s1d7). Os complexos quadráticos são
característicos dos metais de transição com configuração d8.
Geometria tetraédrica
Geometria quadrado planar
109o
90o
[PtCl4]2-
[AuBr4]-
[Co(CN)4]2-
átomo central for pequeno e os
ligantes forem grandes (tais como Cl-,
Br- e I-) ou oxoânions.
[CoCl4]2-
[MnO4]-
[NiCl4]2-
TiCl4
[CuCl4]2-
[Zn(NH3)4]2+](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-25-320.jpg)
![Cisplatina [PtCl2(NH3)2]
Pt(II) quadrado planar
Número de coordenação 4
cis-isômero
primeiro de uma série de compostos de
coordenação de platina usados como drogas anti-câncer
: (Platinol-AQ)
tratamento de câncer por quimioterapia: são utilizados complexos
cis de Pt por conseguirem se ligar ao DNA e ter efeito terapêutico.](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-26-320.jpg)
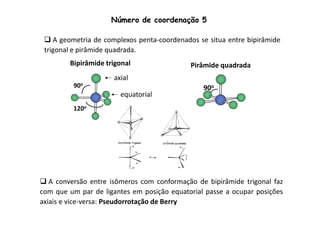
![Número de coordenação 5
A diferença de energia entre as duas formas (bipirâmide trigonal e pirâmide
quadrada) é tão pequena, que o [Ni(CN)5]3- existe com as duas simetrias no
mesmo cristal.
É comum a existência de formas intermediárias.](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-28-320.jpg)
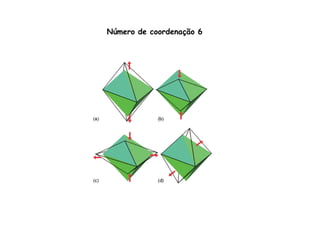
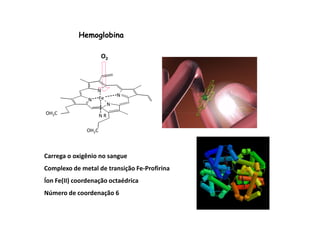
![Número de coordenação 6
são numerosos entre os complexos. Sua geometria é octaédrica, mas
algumas vezes apresenta-se distorcida. É o arranjo mais comum para
metais com configuração d0-d9. Ex.: [Cr(NH3)6]+3 (d3); Mo(CO)6 (d6);
[Fe(CN)6]-3 (d5)
Geometria octaédrica
Geometrica trigonal prismática
Sc(OH2)6]3+
[Cr(NH3)6]
3+
do metais
WMe6
[Mo(CO)6]
[Fe(CN)6]4-](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-29-320.jpg)

![Número de coordenação 7
Octaédro mono-encapuzado
[WBr3(CO)4)]-
(distorcido)
Bipirâmidal pentagonal
D5h
[ZrF7]3-
Prisma trigonal tetragonal/e
encapuzado
[TaF7]2-
comum em metais d mais pesados com altos nox](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-33-320.jpg)
![Número de coordenação 8
antiprisma quadrado Na3[Mo(CN)8]
Dodecaédro
(nBu4N)3[Mo(CN)8]
Número de coordenação 9
Prisma trigonal tri-encapuzado
[ReH9]2-](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-34-320.jpg)


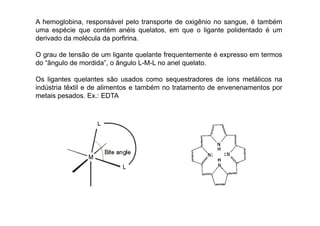
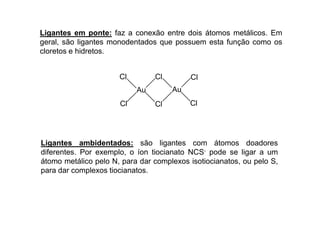

![Representação e nomenclatura
Nomenclatura segundo norma da IUPAC
Composto de coordenação apresenta, normalmente um metal de
transição ao qual se coordenam ligantes, que podem ser iguais ou
diferentes.
Complexo pode ser uma espécie neutra ou um íon (cátion ou ânion).
Fórmula química do complexo colocada entre colchetes
[[CCoo((NNHH3)6]]CCll3](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-40-320.jpg)
![Representação e nomenclatura
Dentro dos colchetes escreve-se o símbolo do metal (átomo central)
e depois os seus ligantes na seguinte ordem:
1º. ligantes negativos (aniônicos)
2º. ligantes neutros (moléculas)
[CoCl2(NH3)4]+: ligante cloreto (negativo) foi escrito antes do ligante
amônia (neutro).
Ligantes positivos (catiônicos) são muito raros, mas, caso exista, deverá
ser escrito por último, após os demais ligantes.](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-41-320.jpg)

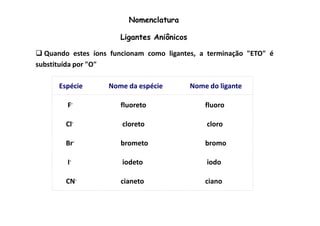

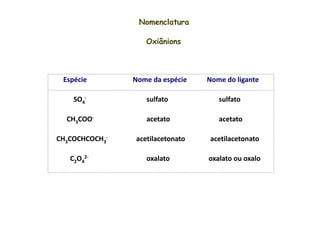
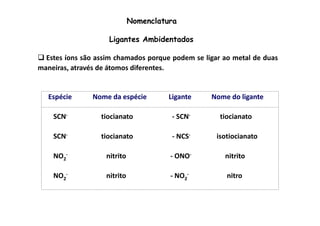
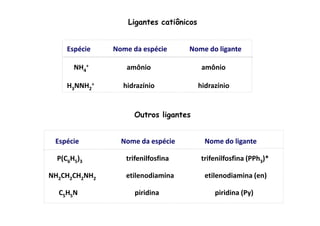

![Nomenclatura de complexos catiônicos e neutros
Para determinar o número de oxidação do metal basta somar as cargas
internas (ligantes dentro dos colchetes), considerando que os ligantes
neutros (moléculas), têm nº de oxidação = zero.
[CoCl2(NH3)4]+ = tetramindiclorocobalto(III)
Nox do cobalto: Co + 2 Cl- + 4 NH3 = +1; Co -2 + 0 = +1; Co = +3
[Co(NO2)(NH3)5](NO3)2 = nitrato de pentaminnitrocobalto(III)
Nox do cobalto: Co + NO2
- + 5 NH3 = +2; Co -1 + 0 = +2; Co = +3
[Ni(CO)4] = tetracarbonilníquel(0)
Nox do níquel: Ni + 4 CO = 0; Ni + 0 = 0; Ni = 0](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-49-320.jpg)
![Nomenclatura de complexos aniônicos
A nomenclatura dos complexos aniônicos é feita da mesma forma, sendo
o metal acrescido da terminação ATO.
[Ni(CN)4]2- = tetracianoniquelato(II)
Nox do níquel: Ni + 4 CN- = - 2; Ni - 4 = - 2; Ni = +2
[Fe(CN) 6]3- = hexacianoferrato(III)
Nox do ferro: Fe + 6 CN- = - 3; Fe - 6 = - 3; Fe = +3
Complexo neutro:
[Pt(Py)4][PtCl4] = tetracloroplatinato(II) de tetrapiridinoplatina(II)
Nox da platina: 2 Pt + 4 Py + 4 Cl- = 0 2 Pt + 0 - 4 = 0 Pt = +2](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-50-320.jpg)

![Nomenclatura de complexos com ligantes em ponte
complexos com ligantes em ponte: normalmente usa-se a letra grega μ
(mi) para indicar um ligante em ponte.
quando esse ligante (L) está ligado a partes iguais (M - L - M), usa-se
prefixos como bis, tris, tetraquis etc para indicar o número de partes
iguais existentes.
NH2
(en) Co(en)2 2Co (SO4)2
OH
sulfato de μ-amido-μ-hidroxo-bis[etilenodiaminacobalto(III)]
Nox do Co: 2 Co + 2 en + NH2
- + OH- = + 4; 2 Co + 0 -1 -1 =+ 4; Co = +3](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-52-320.jpg)
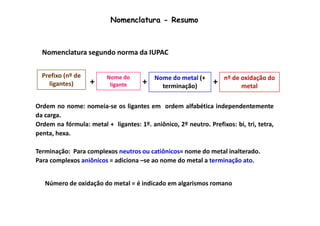
![Nomenclatura - Resumo
Nomes usuais
Nome do ligante: alguns recebem nomes especiais: NH = amin; Cl- = cloro; H O =
3 2aqua; F- = fluoro; CN- = ciano; CO = carbonil; NO = nitrosil.
[Co(en)3]3+ = tris(etilenodiamina)cobalto(III)
bis, tris, tetrakis, hexakis (para indicar o número de partes iguais existentes no
complexo).](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-54-320.jpg)
![Nomenclatura - Exemplos
OH
OH
OH
Co(NH3)3 (NH3)3Co
3+
μ-trihidroxo-bis[triaminocobalto(III)]
Nox do Co: 2 Co + 6 NH3 + 3 OH- = + 3; 2 Co + 0 - 3 =+ 3; Co = + 3
NH2
(NH Fe(CN)2(CO)2 3)4Co Cl2
O
cloreto de μ -amido-μ-oxodicarbonildicianoferrato(III)tetraminocobalto(III)](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-55-320.jpg)
![Nomenclatura - Exemplos
[Cd(SCN)4] 2+ = Tetratiocianatocádmio(II)
[Zn(NCS)4] 2+ = Tetraisotiocianatozinco(II)
[(NH3 )5 Cr -OH- Cr(NH3 )5 ] Cl5
= Cloreto de μ-hidroxo-bis[pentaminocromo(III)
NH4 [Co(SO3)2(NH3)4] = Tetraaminodissulfitocobaltato(III) de amônio
Cis - [PtCl2(Et3P)2] = Cis-diclorodi(trietilfosfino)platina (II)](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-56-320.jpg)
![Nomenclatura - Exemplos
[Co(H2O)6]2+ = hexaaquacobalto(III)
[CoCl4]2- = tetraclorocobaltato(II)
[Ni(CO)4] = tetracarbonilníquel(0)
[Ag(NH3)2]+ = diaminprata(I)
[Al(OH) ]- = tetrahidroxialuminato(III)
4[Co(ONO)(NH3)5]2+ = pentaaminnitritocobalto(III) ONO- = nitrito
NCS- =isotiocianato e SCN- = tiocianato
NO2- = nitro](https://image.slidesharecdn.com/complexosaula11-141211212640-conversion-gate02/85/Complexos-aula-1-1-57-320.jpg)