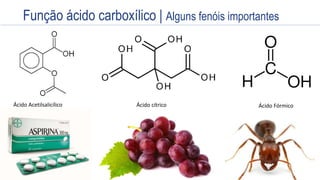
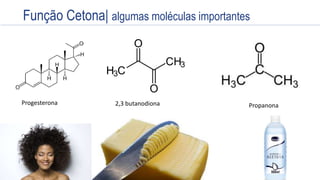
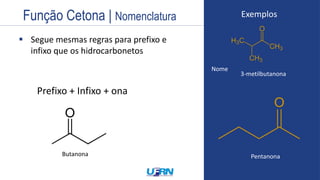
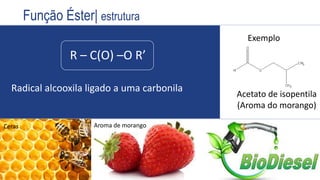
O documento aborda as principais funções oxigenadas na química, incluindo álcoois, éteres, aldeídos, cetonas, ácidos carboxílicos e ésteres. Apresenta também as regras de nomenclatura, propriedades químicas e físicas, reatividade e formas de obtenção desses compostos. O conteúdo é direcionado aos estudantes e visa aprofundar o entendimento sobre a versatilidade e a importância das funções oxigenadas na química orgânica.