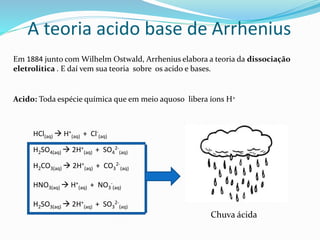
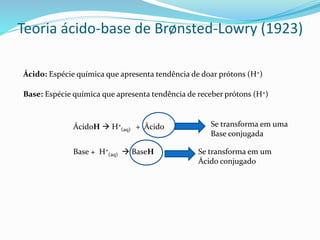
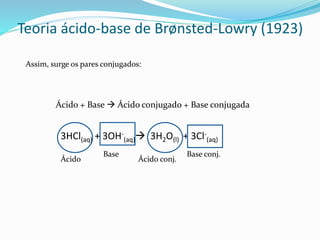
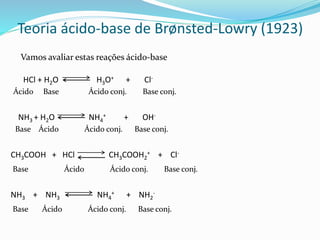
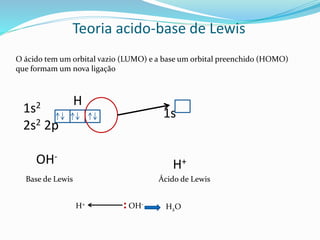
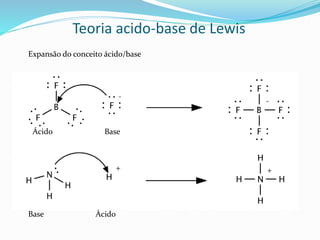
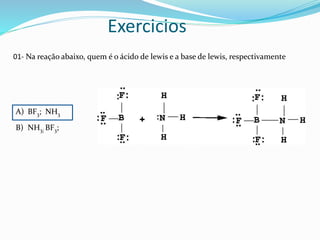
O documento discute as principais teorias ácido-base, incluindo as teorias de Arrhenius, Brønsted-Lowry e Lewis. A teoria de Arrhenius define ácidos como substâncias que liberam íons hidrogênio e bases como substâncias que liberam íons hidroxila em solução aquosa. A teoria de Brønsted-Lowry expande o conceito para incluir a doação e aceitação de prótons. A teoria de Lewis define ácidos e bases com base no compartilhamento de elétrons.