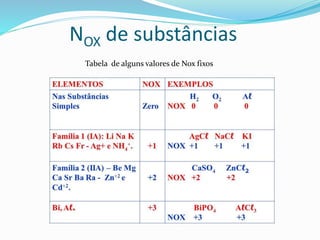
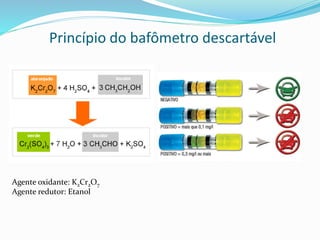
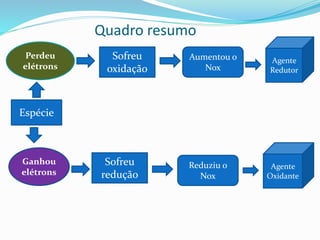
A aula aborda conceitos de oxidação e redução, como: (1) reações de oxidação envolvem perda de elétrons e aumento do número de oxidação, (2) reações de redução envolvem ganho de elétrons e redução do número de oxidação, (3) em reações redox sempre há uma espécie sendo oxidada e outra sendo reduzida. A aula também apresenta exemplos de cálculo de número de oxidação e identificação de agentes oxidantes e redutores.