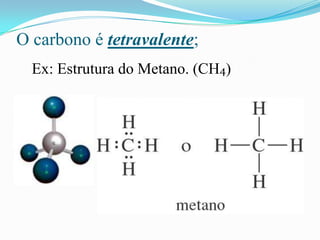
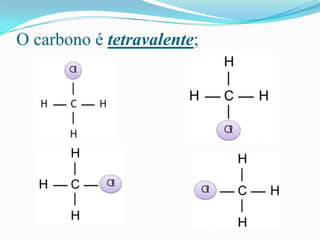
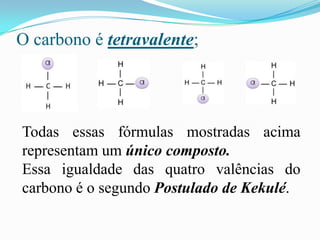
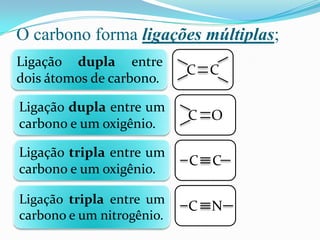
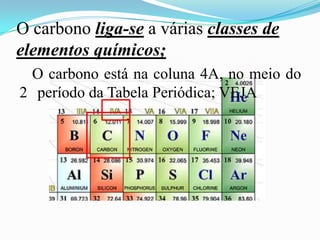
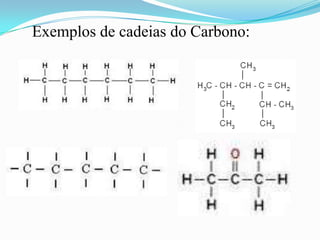
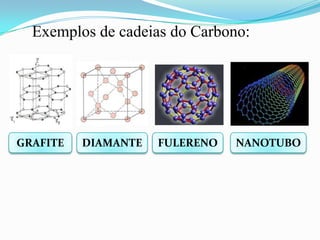
O documento descreve as principais características do átomo de carbono, incluindo sua tetravalência, capacidade de formar ligações múltiplas, ligar-se a diferentes elementos e formar longas cadeias, explicando a habilidade única do carbono em formar inúmeros compostos orgânicos.