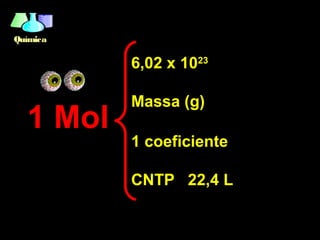
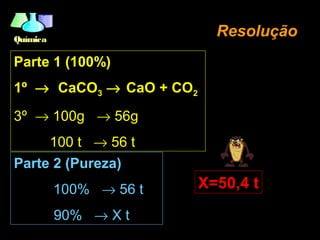
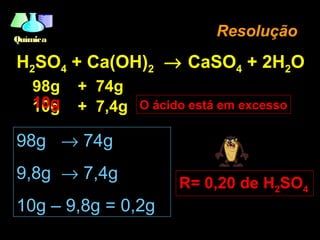
O documento discute os conceitos fundamentais de estequiometria, que é o estudo das relações quantitativas entre as substâncias que participam de uma reação química. Ele apresenta exemplos de cálculos estequiométricos envolvendo relações de massa-massa, massa-moléculas, massa-volume e mol-volume. Também aborda conceitos como rendimento e reagente limitante em reações químicas.