Incorporar apresentação
Baixado 18 vezes




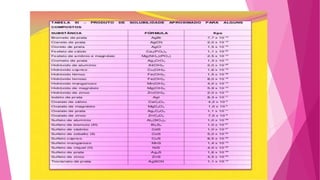




O documento explica o que é produto de solubilidade e constante de solubilidade, denotado por Ks ou PS. Estes valores são constantes para uma solução saturada de um eletrólito pouco solúvel em uma determinada temperatura e são iguais ao produto das concentrações molares dos íons elevados às potências correspondentes aos coeficientes na equação química de dissociação. O documento também fornece exemplos de exercícios para calcular expressões de constante de solubilidade e solubilidade para diferentes compostos.







