Este documento discute os conceitos fundamentais de estequiometria, incluindo:
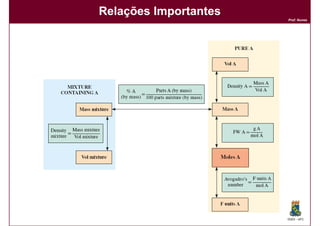
1) O conceito de mol e número de Avogadro e como eles se relacionam com massas atômicas;
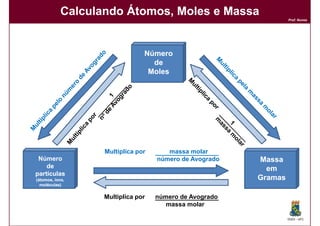
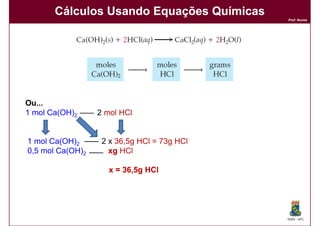
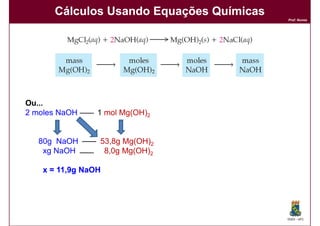
2) Como converter entre números de átomos, moles e massas;
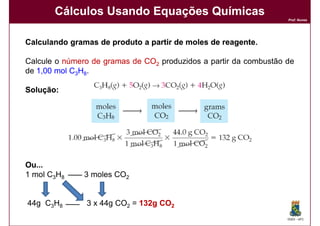
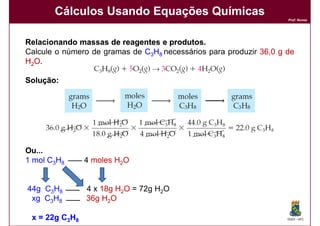
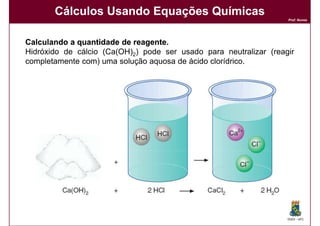
3) A função e importância das equações químicas balanceadas para cálculos químicos.