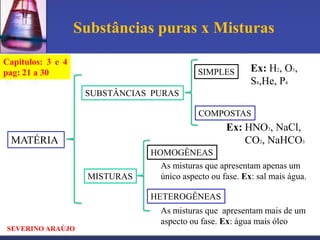
Este documento apresenta informações sobre substâncias químicas puras e misturas. Discute a diferença entre substâncias puras e misturas, tipos de misturas, número de fases em sistemas e processos para separar componentes de misturas, como filtração, decantação e destilação.