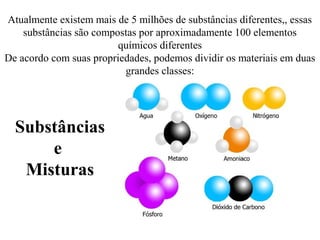
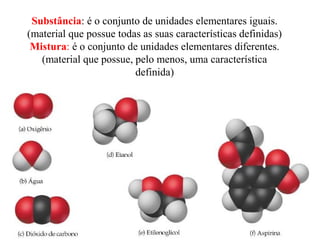
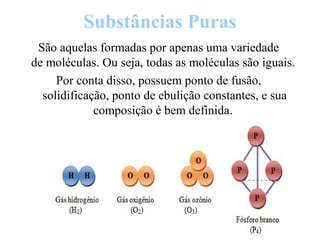
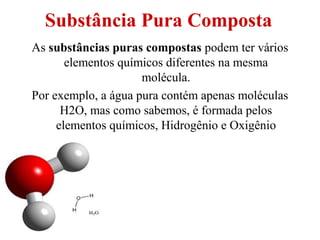
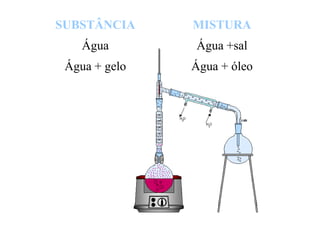
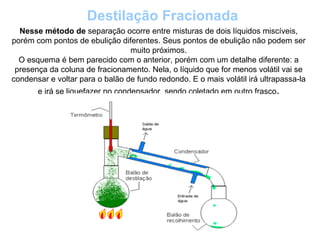
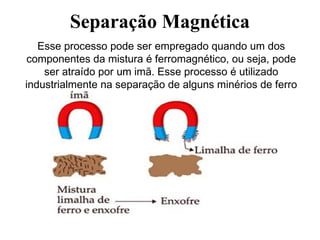
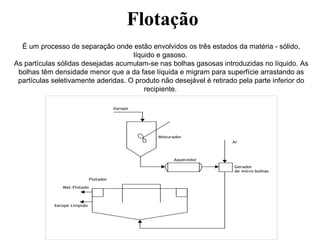
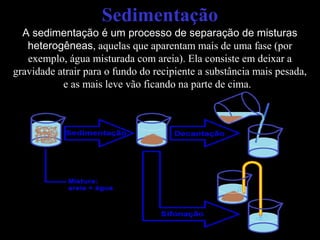
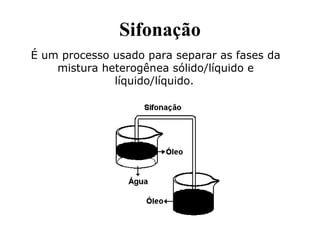
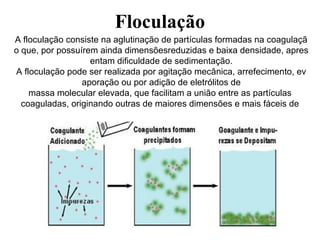
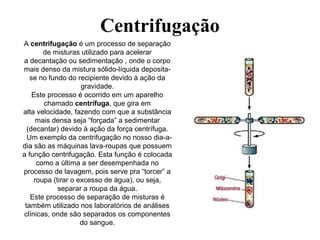
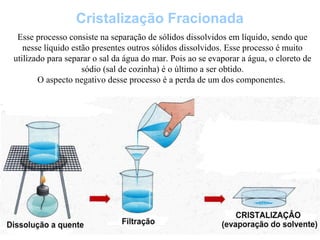
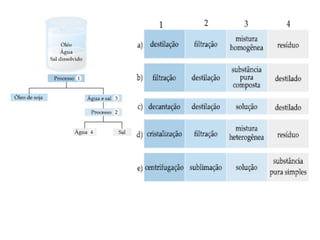
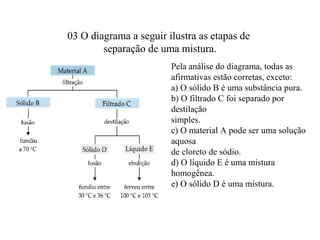
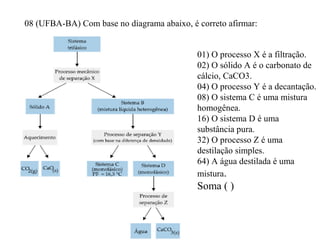
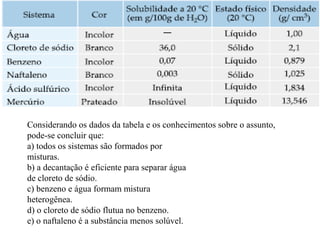
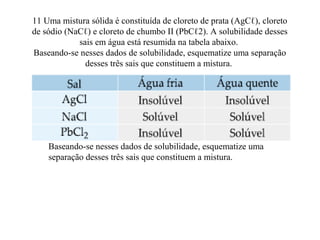
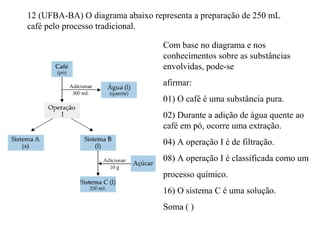
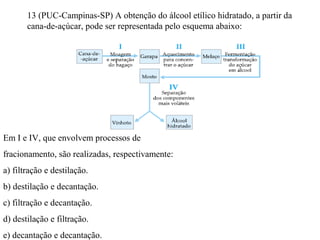
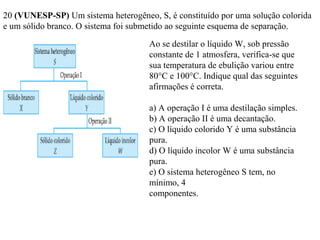
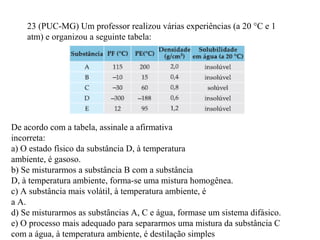
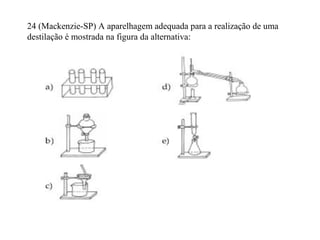
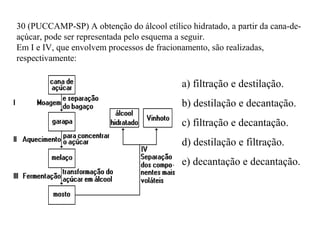
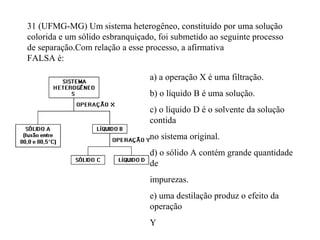
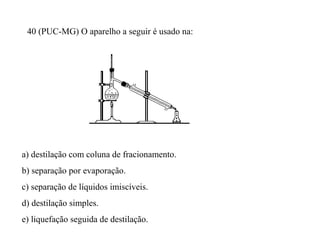
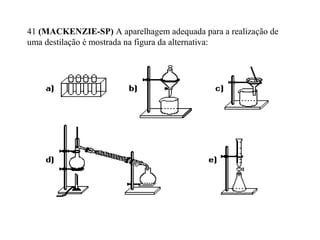
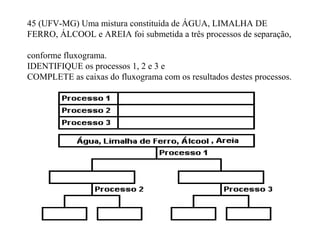
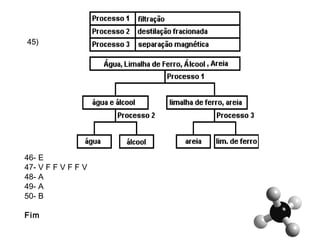
O documento discute substâncias e misturas, definindo-as como conjuntos de unidades elementares iguais ou diferentes, respectivamente. Substâncias podem ser puras ou compostas, e misturas podem ser homogêneas ou heterogêneas. Vários métodos são descritos para separar componentes de misturas, como destilação, extração por solventes e cromatografia.