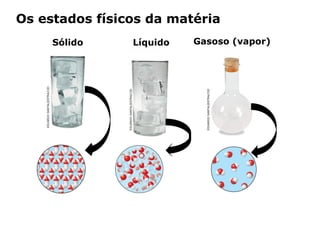
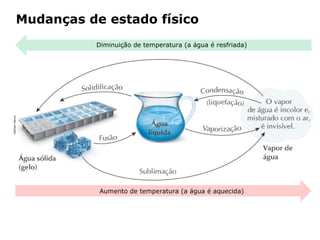
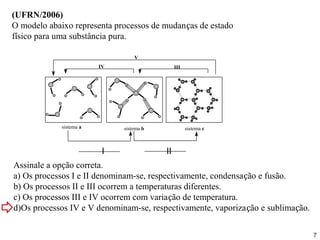
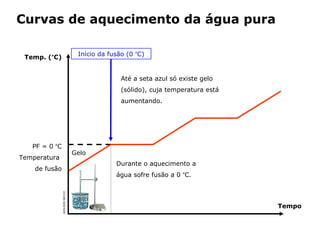
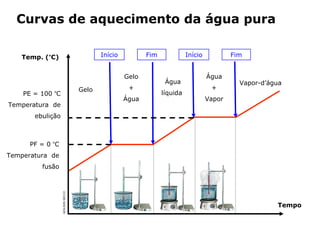
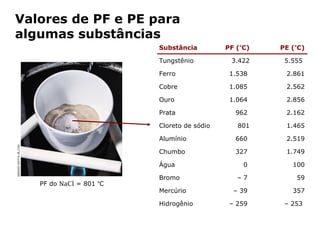
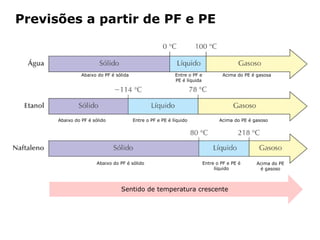
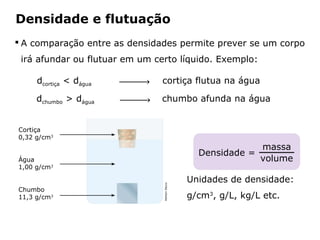
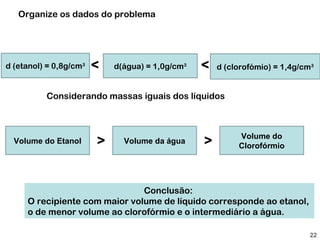
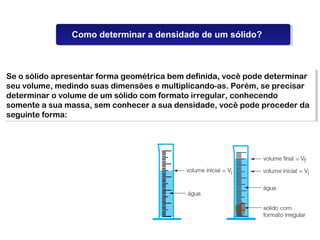
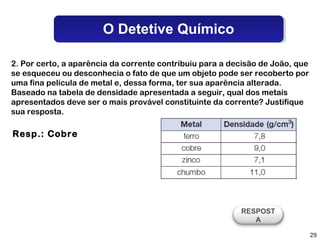
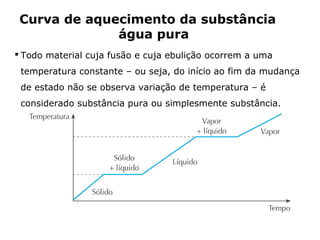
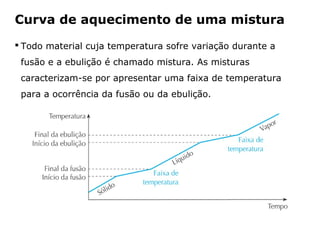
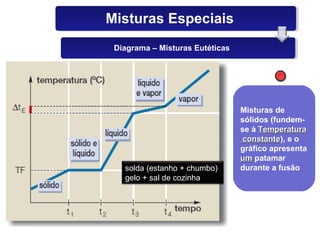
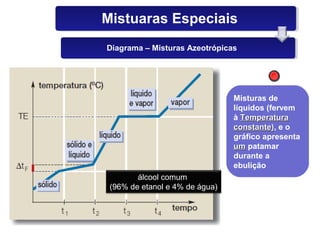
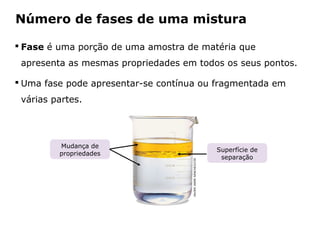
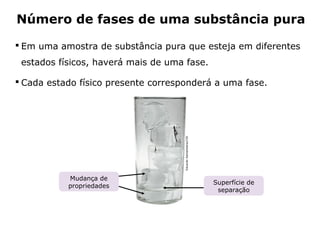
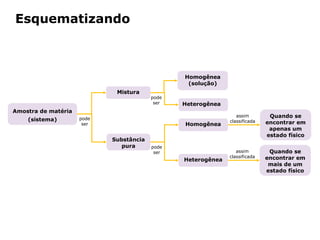
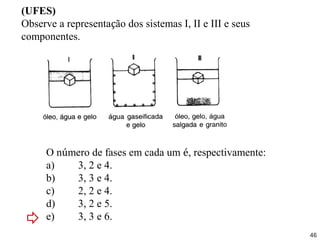
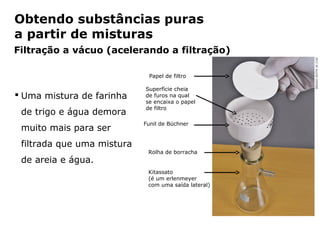
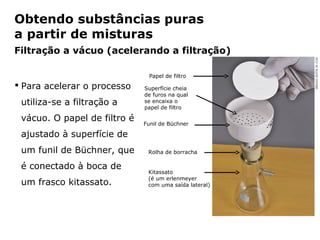
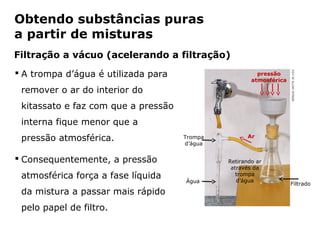
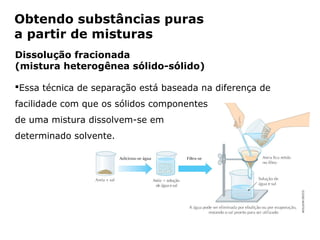
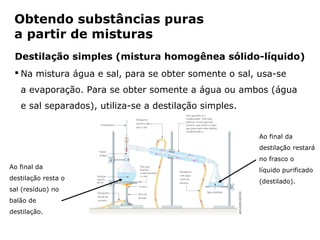
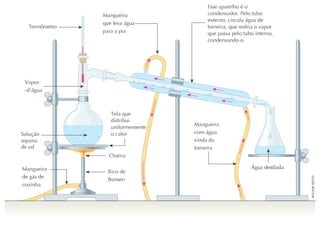
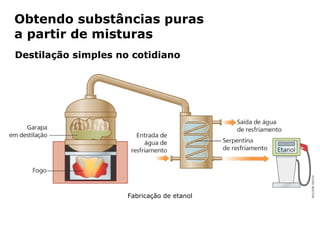
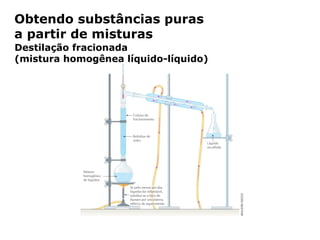
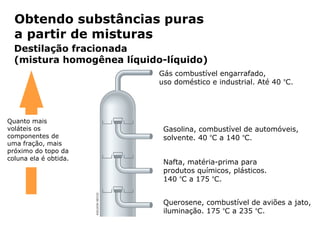
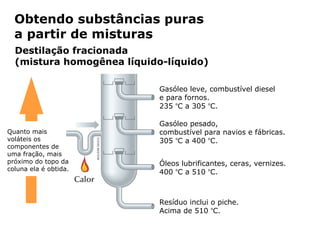
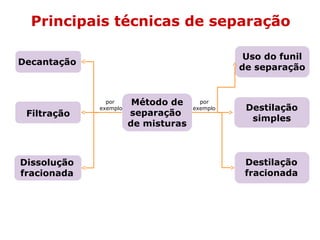
O documento discute os estados físicos da matéria e as mudanças entre eles. Apresenta exemplos como:
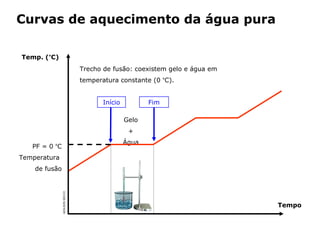
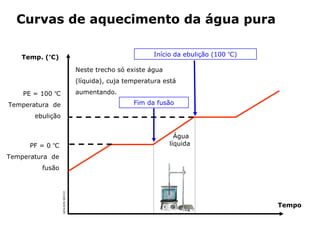
1) O gelo derrete e se torna água líquida quando aquecido até 0°C.
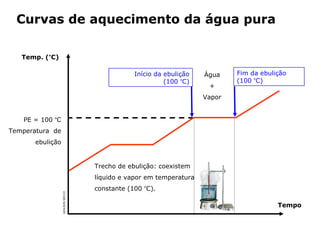
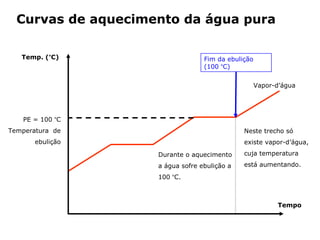
2) A água ferve e se torna vapor quando aquecida até 100°C.
3) As substâncias podem existir nos estados sólido, líquido ou gasoso dependendo da temperatura.