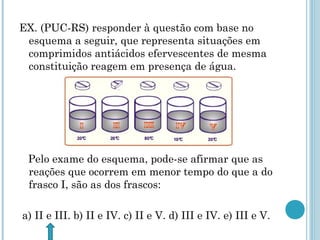
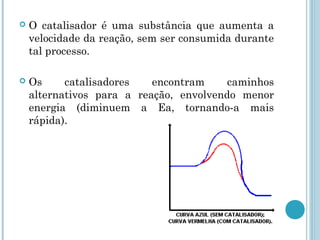
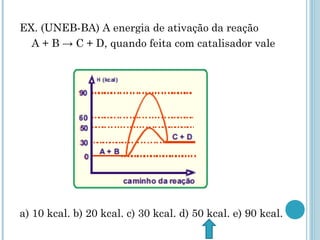
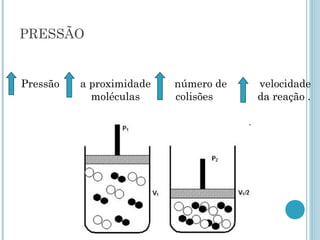
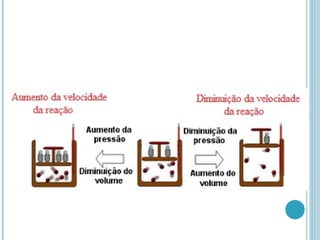
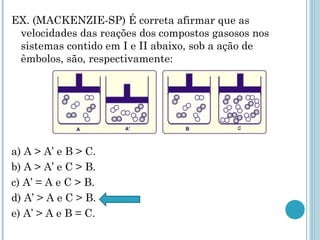
O documento discute os conceitos fundamentais da cinética química, incluindo:
1) A cinética química estuda a velocidade das reações químicas e os fatores que as influenciam, como a temperatura e a presença de catalisadores.
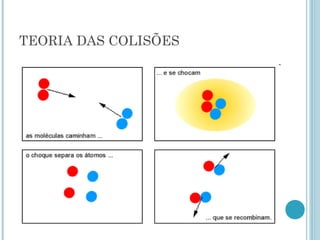
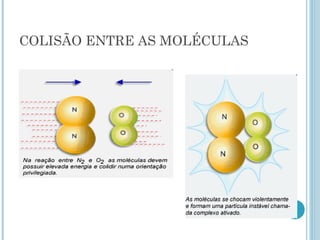
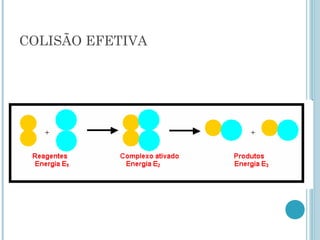
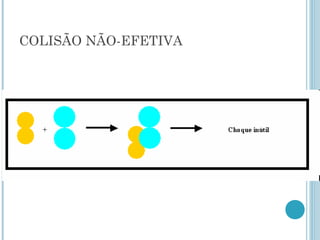
2) A teoria das colisões explica que as reações ocorrem quando as moléculas colidem com energia suficiente para romper ligações químicas e formar novos compostos.
3) Fatores como a concentração dos reagentes, área de contato








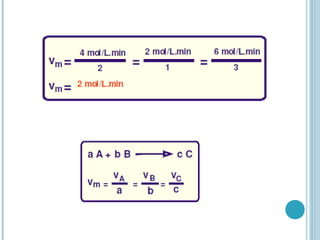


![V = k [A]a
. [B]b
V = velocidade da reação;
[ ] =concentração da substância em mol / L;
k = constante da velocidade específica para cada
temperatura.](https://image.slidesharecdn.com/aula10cinticaqumica-150810002044-lva1-app6892/85/Cinetica-Quimica-19-320.jpg)

![Observe os dados:
- Entre os experimentos 1 e 2, a [CO] dobrou e a velocidade não foi modificada.
A velocidade da reação não depende da [CO].
•- Entre os experimentos 2 e 3, a [NO2] dobrou e a velocidade quadruplicou.
Velocidade aumenta quatro vezes quando dobra a [NO2].](https://image.slidesharecdn.com/aula10cinticaqumica-150810002044-lva1-app6892/85/Cinetica-Quimica-21-320.jpg)
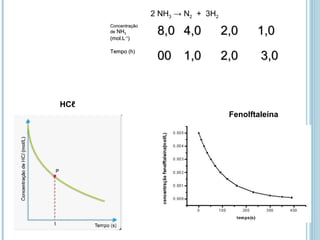
![EX. óxido nítrico reage com hidrogênio, produzindo
nitrogênio e vapor de água de acordo com a reação:
2 NO (g) + 2 H2 (g) N2 (g) + 2 H2O (g)
Acredita-se que essa reação ocorra em duas etapas:
2 NO + H2 N2O + H2O (lenta)
N2O + H2 N2 + H2O (rápida)
De acordo com esse mecanismo, a expressão da
velocidade da reação é:
a)v = k [NO]2 [H2]. b) v = k [NO2][H2O].
c) v = k [NO][H2]. d) v = k [N2][H2O].
e) v = k [N2][H2O]2 .](https://image.slidesharecdn.com/aula10cinticaqumica-150810002044-lva1-app6892/85/Cinetica-Quimica-22-320.jpg)




![ Quanto maior a concentração dos reagentes,
maior será a velocidades da reação.
O carvão na churrasqueira quando abanado fica
incandescente porque estamos aumentando a [ ]
de gás oxigênio (O2 , que é reagente na
combustão), portanto aumenta a velocidade da
reação.
CONCENTRAÇÃO DOS REAGENTES](https://image.slidesharecdn.com/aula10cinticaqumica-150810002044-lva1-app6892/85/Cinetica-Quimica-27-320.jpg)