I. O documento descreve fatores que afetam a velocidade de reações químicas, como a temperatura, concentração dos reagentes e presença de catalisadores.
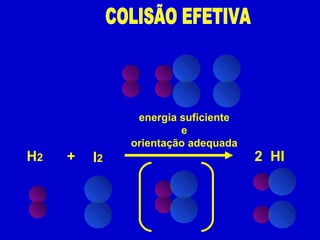
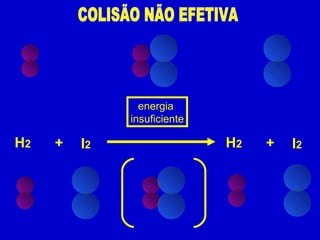
II. A velocidade de uma reação depende da frequência e energia das colisões entre moléculas, que por sua vez são influenciadas por esses fatores.
III. A lei da velocidade relaciona a velocidade de uma reação elementar à concentração dos reagentes elevados a exponentes iguais aos coeficientes estequiométricos.

![É a maior ou menor rapidez (velocidade)
com que uma reação ocorre
É calculada pela relação entre a quantidade
de um reagente (ou produto) que é consumido (ou produzido)
e o intervalo de tempo gasto para isto
[ final ] – [ inicial ]
VM =
t final – t inicial](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-2-320.jpg)
![As quantidades das substâncias
são medidas em
mol/L, massas, volumes (gases), etc.,
A quantidade de reagente ou produto
medida em mol/L é representada por [ ]
Enquanto que o intervalo de tempo pode ser dado em
segundos, minutos ou horas](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-3-320.jpg)




















![Para uma reação genérica: a A + b B Produtos
A velocidade da reação é dada pela expressão:
x y
v=k[A] [B]
Onde os valores de “ x ” e “ y ”
são determinados experimentalmente
Esta equação é conhecida pelo nome de
LEI DA VELOCIDADE](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-27-320.jpg)
![Para as reações ELEMENTARES
os valores dos expoentes são iguais aos coeficientes das
substâncias na equação química
Para a reação:
2 NO (g) + H2 (g) N2O (g) + H2O (g)
A lei da velocidade é:
v = k [ NO ] 2 [ H2 ]](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-28-320.jpg)
![01) A reação A + 2 B P se processa em uma única etapa. Qual a
velocidade desta reação quando K = 0,3 L/mol . min, [A] = 2,0 M e
[B] = 3,0 M ?
k = 0,3 L / mol . min
a) 5,4.
[ A ] = 2,0 M
b) 4,5.
[ B ] = 3,0 M
c) 1,8.
d) 18,0. v = k[A] [B] 2
2
e) 54. v = 0,3 x 2 x 3 v = 0,3 x 2 x 9
vv = 5,4
= 5,4](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-29-320.jpg)
![Se uma reação ocorrer em várias etapas
sua velocidade é dada pela
ETAPA MAIS LENTA
A + A A2 ( etapa lenta )
A 2 + B A 2B ( etapa rápida )
2 A + B A 2B ( reação global )
A lei da velocidade é: 2
A lei da velocidade é: V = k[A]](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-30-320.jpg)
![02) (Unip-SP) A poluição é uma das causas da destruição da camada de ozônio.
Uma das reações que podem ocorrer no ar poluído é a reação do dióxido de
nitrogênio com o ozônio:
2 NO2 (g) + O3 (g) N2O5 (g) + O2 (g)
Pág. 45
Essa reação ocorre em duas etapas:
Ex. 11
I. NO2 (g) + O3 (g) NO3 (g) + O2 (g) (lenta)
II. NO3 (g) + NO (g) N2O5 (g) (rápida)
Assinale a lei de velocidade para essa reação:
a) v = k [NO2] 2 [O3]
b) v = k [NO2] [O3]
c) v = k [NO3] [NO2]
d) v = k [NO2] [O3] + k’ [NO3] [NO2]
e) v = k [NO2] 2](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-31-320.jpg)
![03) Na decomposição térmica da amônia expressa pela equação:
2 NH3 (g) N2 (g) + 3 H2 (g)
Duplicando-se a concentração molar de NH 3, a velocidade da
reação ficará: v = k [ NH3 ] 2
a) inalterada.
[ NH3 ] = x mol /L
b) duas vezes maior.
c) três vezes maior. v = k x 2
d) quatro vezes maior.
[ NH3 ] = 2x mol /L
e) seis vezes maior.
v’ = k ( 2x ) 2
v’ = 4 k x 2
v’ = 4 v](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-32-320.jpg)

![04) Unisinos-RS) Na Química ambiental, que procura, entre outras coisas, avaliar
formas de atenuar a emissão de substâncias gasosas que depreciam a
qualidade do ar; a reação entre os gases monóxido de carbono e oxigênio,
para produzir dióxido de carbono, tem grande importância. A equação
representativa dessa reação é: v1
2 CO (g) + O2 (g) 2 CO2 (g) Pág. 45
v2 Ex. 10
Quando se duplicarem, simultaneamente, as concentrações molares de CO
e O2, efetuando a reação em sistema fechado, por quantas vezes ficará
multiplicada a velocidade da reação “v”?
2
v = k [CO] [O2]
a) 2.
b) 4.
[CO2] = x mol/L [CO2] = 2x mol/L
c) 8.
[O2] = y mol/L [O2] = 2y mol/L
d) 16.
2 2
v=kx y v’ = k (2x) (2y)
e) 32.
2
v’ = 8 k x y
v](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-34-320.jpg)
![05) A tabela abaixo apresenta os valores das velocidades de reação e as
correspondentes concentrações em mol / L dos reagentes em idênticas
condições, para o processo químico representado pela equação:
3X + 2Y Z + 5W
Pág. 44
velocidade [X] [Y]
Ex. 08
1 10 5 10
2 40 10 10
3 40 10 20
a b
Qual a equação de velocidade desse processo? v = k [X] [Y]
a b 2 b
2 40 k x 10 x 10 3 40 k x 10 x 20
= =
1 a b 2 2 b
10 k x 5 x 10 40 k x 10 x 10
a b
4 = 2 1 = 2
2 a 0 b
2 = 2 2 = 2
a = 2 b = 0
2 0 2
v = k [X] [Y] ou v = k [X]](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-35-320.jpg)
![06) (Urca-CE) Dada a seguinte reação genérica “2 A + B C” e o quadro cinético
abaixo:
Experiência [A] m L
ol/ [B] m L
ol/ Velocidade (m L.s)
ol/
I 0,42 0,21 0,20
II 0,42 0,63 1,80
III 0,84 0,21 0,40
É correto afirmar:
x y
a) é uma reação elementar. v = k [A] [B]
b) a ordem global da reação é 2.
v = k [A] [B] 2
c) a lei de velocidade é v = k[A] 2[B].
d) a constante de velocidade é igual a 1.
e) a lei de velocidade é v = k[A][B] 2.
2 1,80 x y
k . (0,42) (0,63) y
= x y 9 = 3 y=2
1 0,20 k . (0,42) (0,21)
3 0,40 x y
k . (0,84) (0,21) x
= y 2 = 2 x=1
1 0,20 k . (0,42) x (0,21)](https://image.slidesharecdn.com/cinetica-121203071636-phpapp01/85/Cinetica-36-320.jpg)
