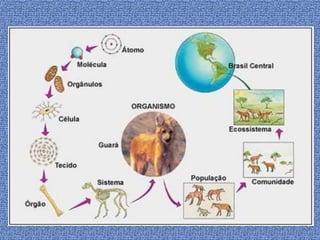
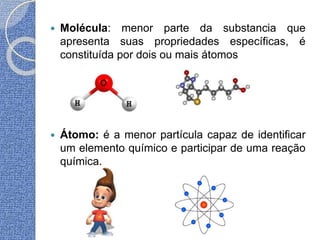
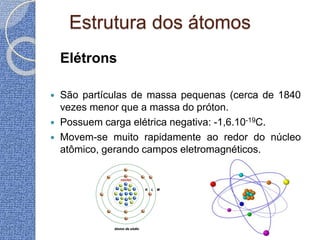
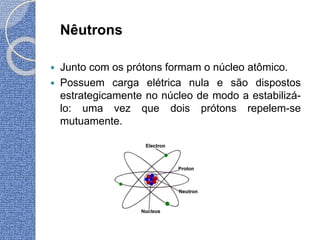
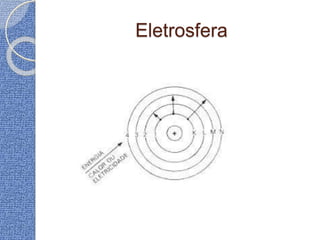
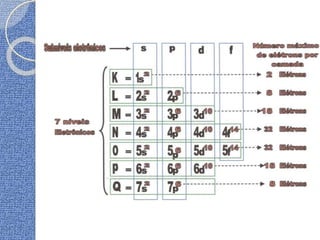
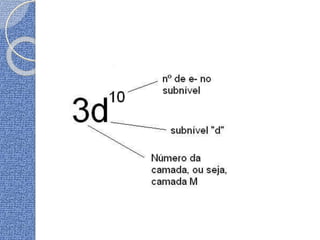
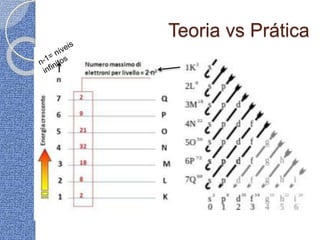
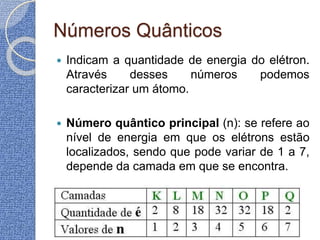
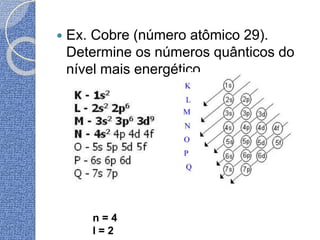
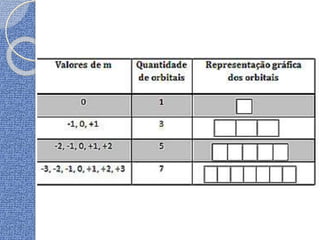
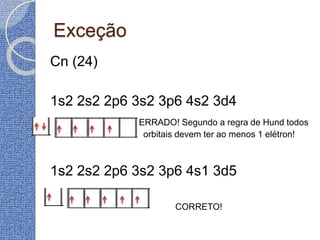
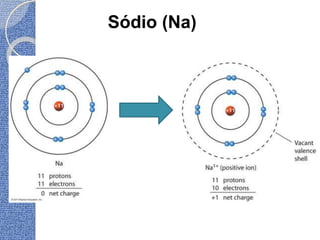
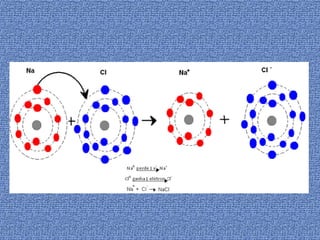
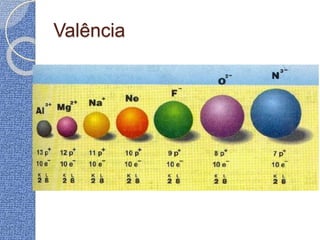
O documento discute conceitos básicos de átomos e estrutura atômica, incluindo: (1) a definição de átomo como a menor partícula capaz de identificar um elemento químico, (2) a estrutura interna do átomo composta por elétrons, prótons e nêutrons, e (3) os números quânticos que caracterizam os elétrons e níveis de energia dentro do átomo.