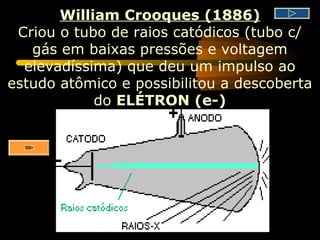
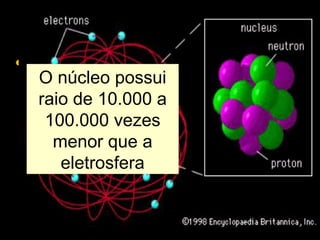
O documento apresenta informações sobre a história do modelo atômico, desde as primeiras teorias de Demócrito e Dalton até os modelos atômicos modernos. Resume os principais modelos propostos por cientistas como Thomson, Rutherford e Bohr e conceitos-chave como elétrons, prótons, nêutrons e números quânticos.