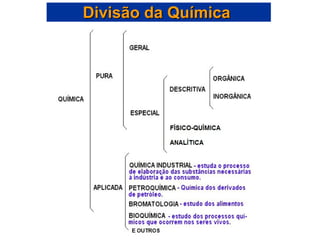
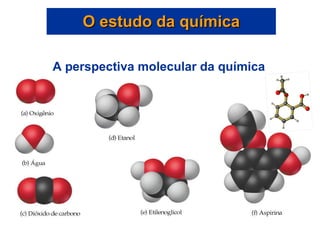
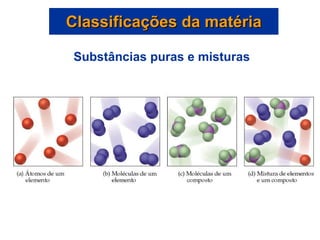
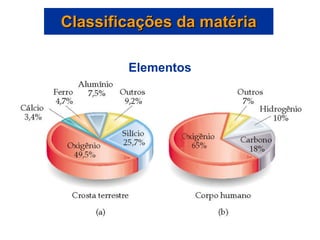
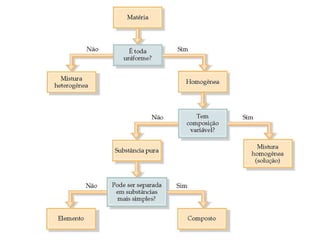
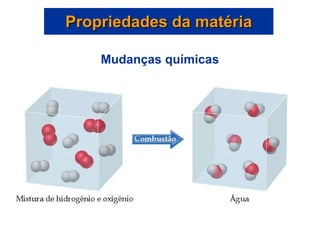
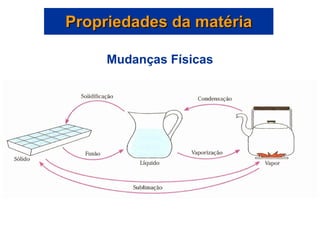
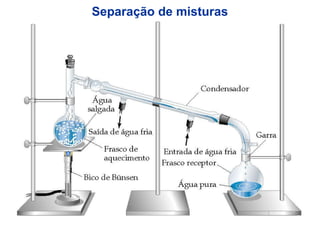
Este documento discute os conceitos básicos da química, incluindo os três estados da matéria, as classificações de substâncias puras e misturas, e os elementos e compostos que constituem a matéria. Também aborda as propriedades físicas e químicas da matéria, além de métodos para separar misturas como filtração e destilação.