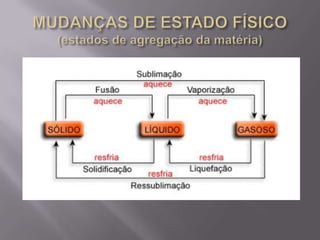
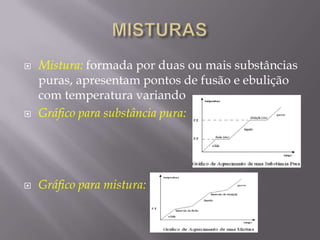
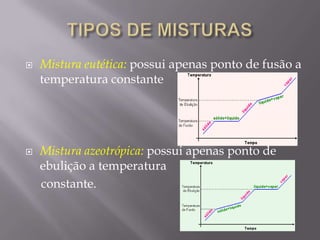
O documento discute conceitos básicos de química, incluindo transformações da matéria através de reações químicas e mudanças de estado físico. Também aborda classificações de substâncias, tipos de misturas e métodos de separação de misturas como filtração, decantação e destilação.