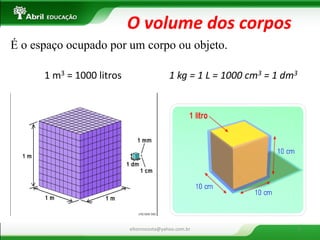
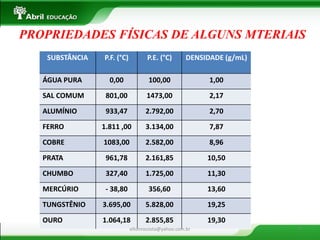
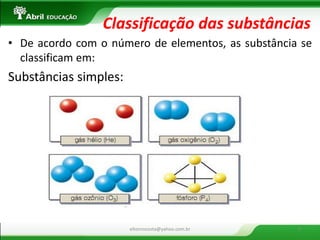
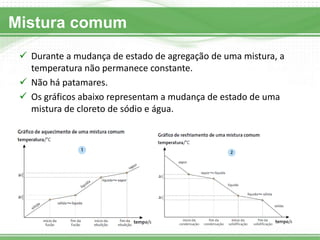
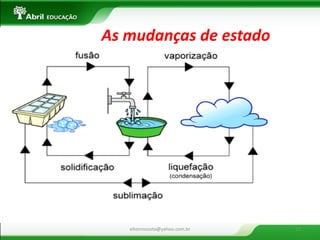
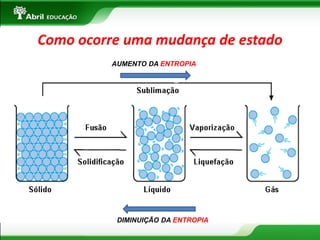
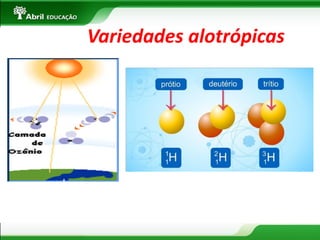
O documento apresenta uma introdução sobre sistemas físicos, energia e suas propriedades. Aborda os conceitos de sistema, energia cinética e potencial. Discute também a diferença entre energia e força, além dos tipos de força existentes. Por fim, explica conceitos como massa, volume, densidade e classificação de substâncias.