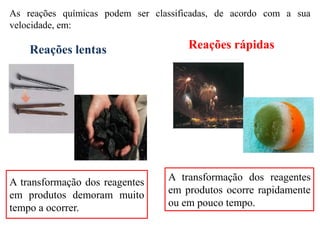
O documento discute fatores que influenciam a velocidade de reações químicas, incluindo temperatura, concentração de reagentes, estado de divisão de sólidos, luz e catalisadores. Reações podem ocorrer lentamente, como formação de combustíveis fósseis, ou rapidamente, como reações ácido-calcário. A velocidade geralmente aumenta com temperatura e concentração mais altas.