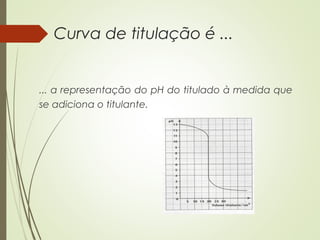
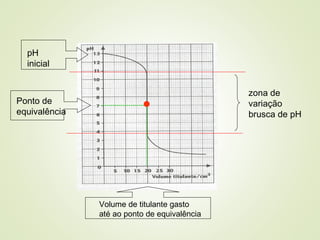
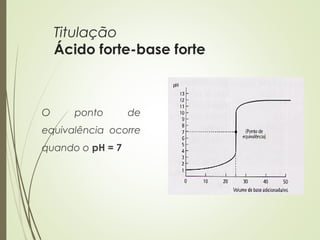
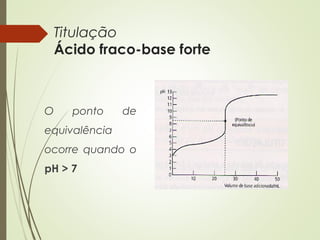
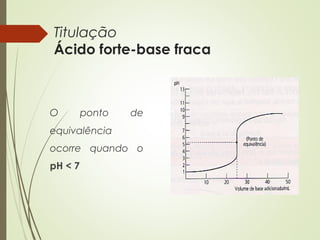
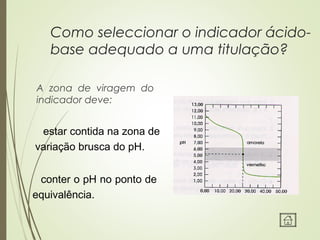
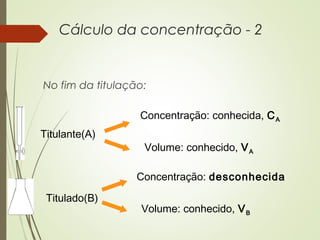
Este documento discute titulações ácido-base, incluindo o que é uma titulação, como se executa, e como se detecta o ponto de equivalência. Uma titulação envolve a adição de uma solução de concentração conhecida (titulante) a uma solução de concentração desconhecida (titulado) até o ponto de equivalência, quando as quantidades de ácido e base são estequiométricamente iguais.