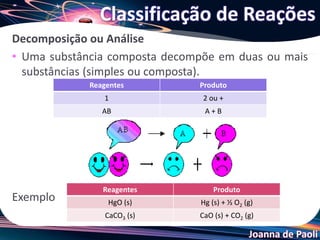
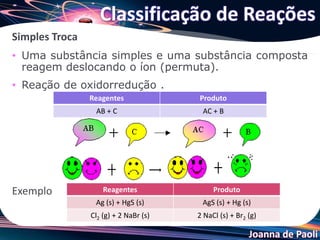
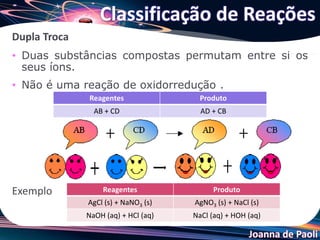
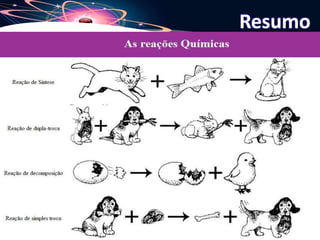
O documento discute as características e classificações de reações químicas. Ele define reação química e lista evidências de sua ocorrência. Também explica equações químicas, simbologias, e classifica reações em síntese, decomposição, simples troca e dupla troca com exemplos.