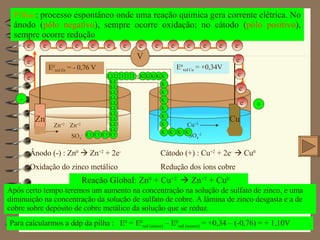
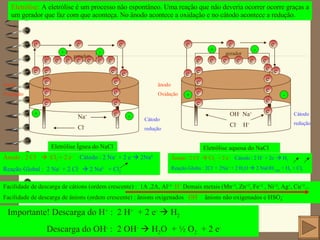
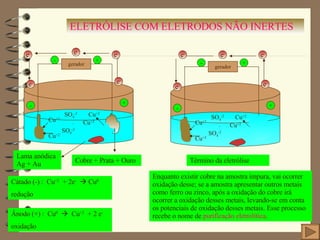
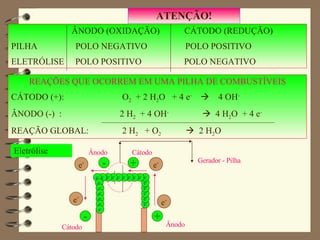
O documento resume conceitos importantes de eletroquímica, incluindo oxidação, redução, diferença de potencial, pilhas, eletrólise e aspectos quantitativos. Oxidação envolve perda de elétrons e redução envolve ganho de elétrons. Pilhas geram corrente elétrica através de reações espontâneas de oxirredução, enquanto a eletrólise requer um gerador externo para fazer reações não espontâneas acontecerem.