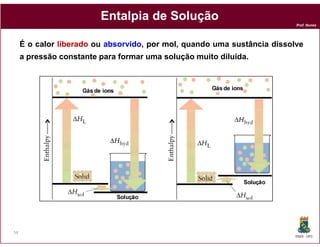
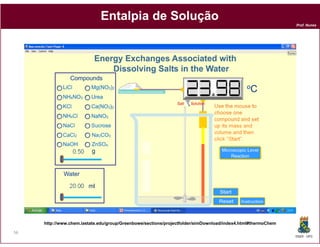
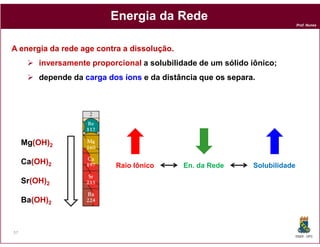
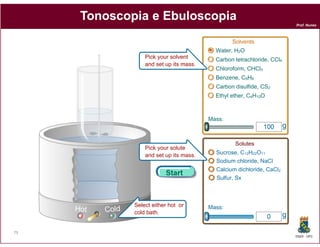
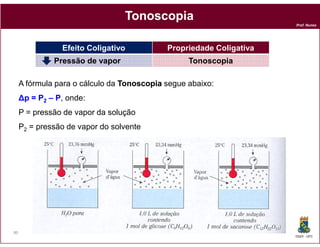
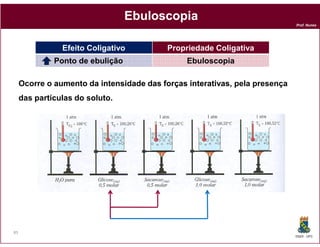
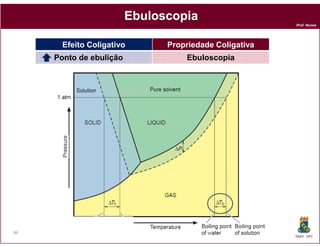
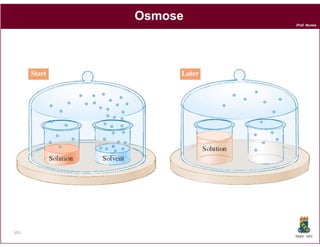
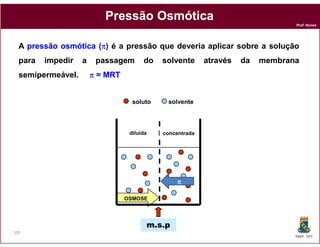
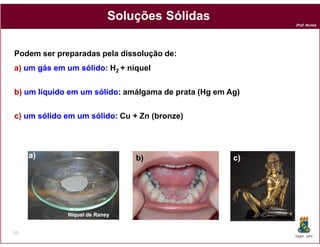
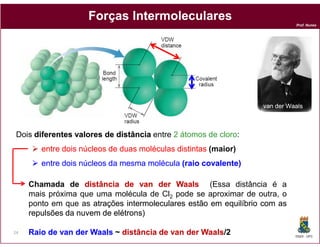
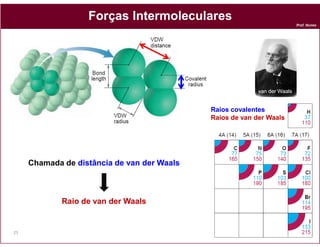
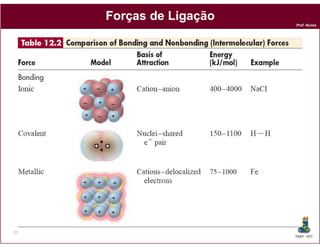
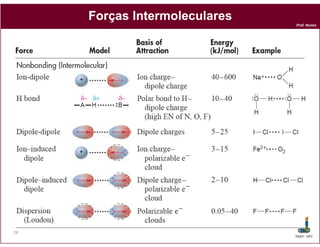
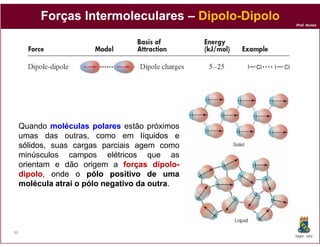
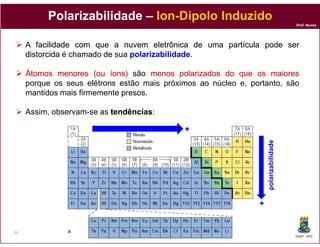
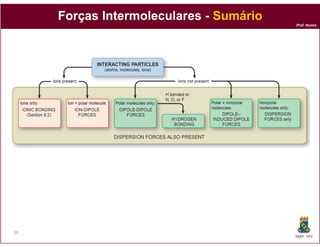
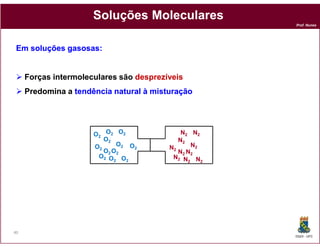
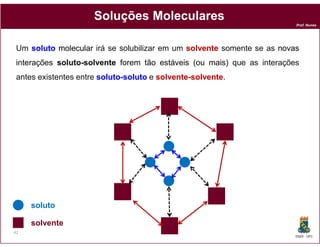
Este documento discute os conceitos fundamentais de soluções químicas. Ele define soluções como misturas homogêneas onde o soluto e o solvente estão misturados em uma única fase. O documento também discute os componentes de uma solução, tipos de soluções, concentrações de soluções e os fatores que afetam a solubilidade, incluindo as forças intermoleculares entre o soluto e o solvente.






































![Produto de Solubilidade - KPs
Prof. Nunes
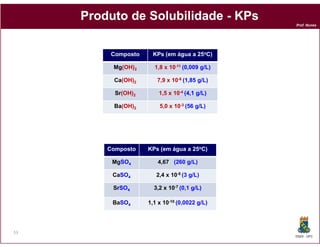
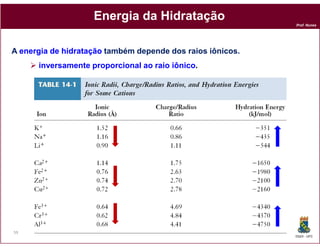
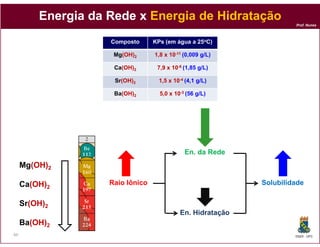
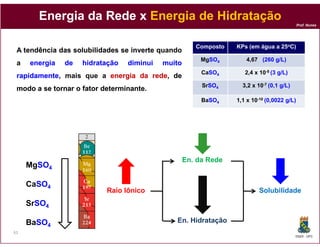
A solubilidade de um composto pode ser quantificada através de sua
constante de solubilidade – KPs.
A 2 B (s ) 2 A + (a q ) + B - - (a q )
H 2O
KPs = [A+]2 x [B-2]
Composto KPs (em água a 25oC)
Cloreto de chumbo(II) (PbCl2) 1,17 ×10–5
Cloreto de prata (AgCl) 1,77 ×10–10
Hidróxido de ferro(II),Fe(OH)2 4,87 ×10–18
Sulfureto de prata (I) (Ag2S) 6,0 ×10–30
Fonte: CRC Handbook of Chemistry and Physics, 76th edition, CRC Press, INC, 1996
52
DQOI - UFC](https://image.slidesharecdn.com/solucoes-110921134828-phpapp02/85/Solucoes-Quimicas-52-320.jpg)