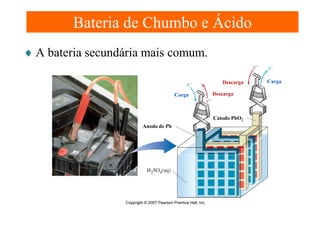
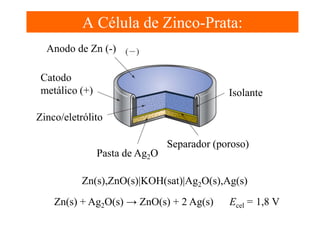
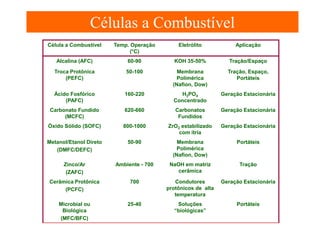
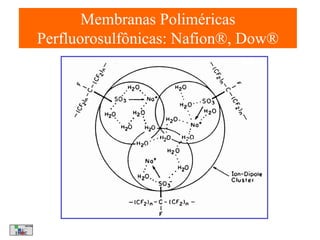
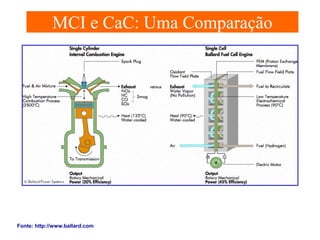
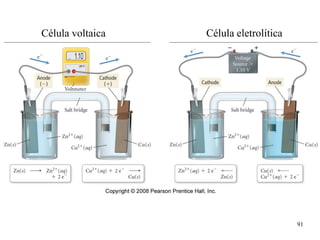
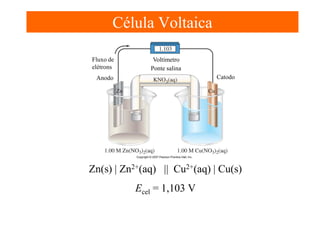
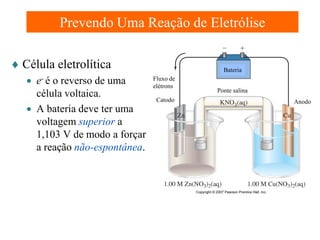
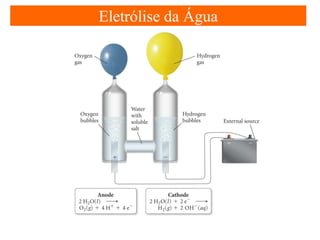
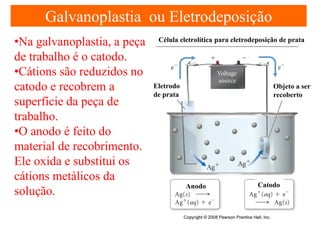
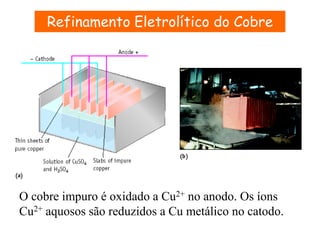
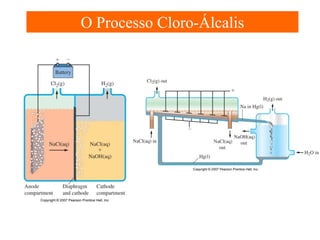
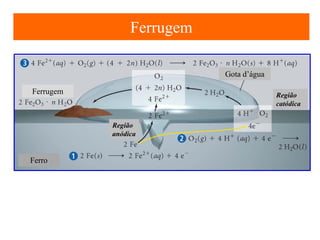
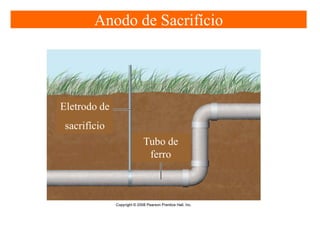
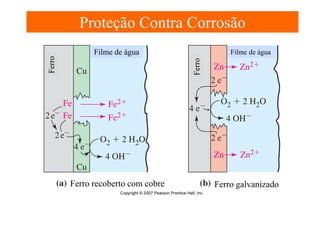
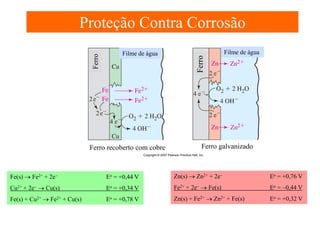
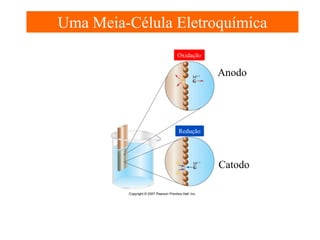
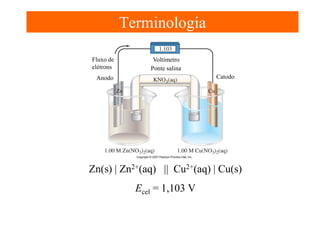
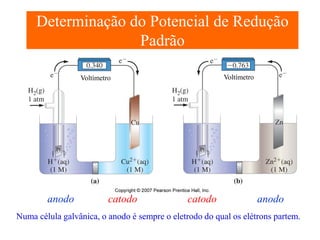
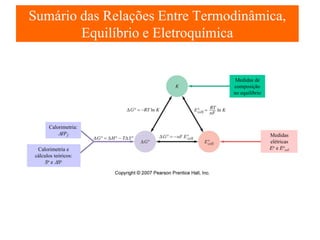
O documento apresenta um resumo sobre eletroquímica, abordando conceitos como reações eletroquímicas, números de oxidação, potenciais de eletrodo, baterias, corrosão e eletrólise. O texto também discute a importância do estudo da eletroquímica para processos industriais e biológicos.






























![Uma Célula Eletroquímica
Voltímetro
Ponte Salina [KNO3(aq)]](https://image.slidesharecdn.com/eletroquimica-131105082925-phpapp01/85/Eletroquimica-34-320.jpg)





















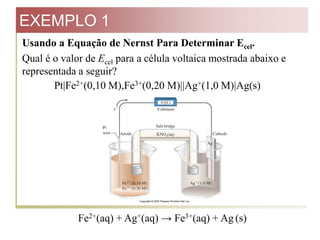
![EXEMPLO 1
Pt|Fe2+(0,10 M),Fe3+(0,20 M)||Ag+(1,0 M)|Ag(s)
Fe2+(aq) + Ag+(aq) → Fe3+(aq) + Ag (s)
0,0592 V
Ecell = Ecell° log Q
n
0,0592 V
[Fe3+]
log
Ecell = Ecell° [Fe2+] [Ag+]
n
Ecell = 0,029 V – 0,018 V = 0,011 V](https://image.slidesharecdn.com/eletroquimica-131105082925-phpapp01/85/Eletroquimica-60-320.jpg)

![EXEMPLO 2
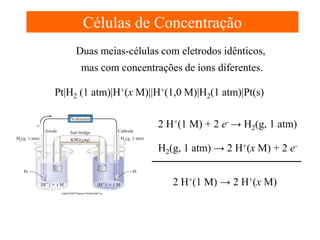
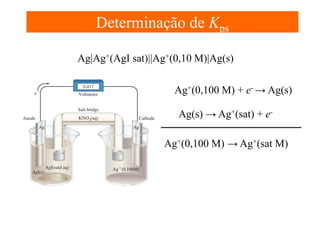
Usando uma Célula Voltaica Para Determinar a Kps de um
Sal Pouco Solúvel. Com os dados das reação do slide anterior,
calcule a Kps para AgI.
AgI(s) → Ag+(aq) + I-(aq)
Seja x = [Ag+] em uma solução saturada de Ag+:
Ag+(0,100 M) → Ag+(sat M)
0,0592 V [Ag+]AgI sat
0,0592 V
log
log Q = Ecell° Ecell = Ecell° [Ag+] sol. 0,10 M
n
n](https://image.slidesharecdn.com/eletroquimica-131105082925-phpapp01/85/Eletroquimica-64-320.jpg)
![EXEMPLO 2
0,0592 V [Ag+]AgI sat
Ecell = Ecell° log
[Ag+] sol. 0,10 M
n
x
0,0592 V
Ecell = Ecell° log
0,100
n
0,0592 V
(log x – log 0,100)
0,417 = 0 1
0,417
log x = log 0,100 = -1 – 7,04 = -8,04
0,0592
x = 10-8,04 = 9,1×10-9
Kps = x2 = 8,3×10-17](https://image.slidesharecdn.com/eletroquimica-131105082925-phpapp01/85/Eletroquimica-65-320.jpg)


![A Célula de Leclanché (Seca)
Zn(s) → Zn2+(aq) + 2 e-
Oxidação:
Redução:
2 MnO2(s) + H2O(l) + 2 e- → Mn2O3(s) + 2 OH-
Reação ácido-base:
NH4+ + OH- → NH3(g) + H2O(l)
Reação de precipitação:NH3 + Zn2+(aq) + Cl- → [Zn(NH3)2]Cl2(s)](https://image.slidesharecdn.com/eletroquimica-131105082925-phpapp01/85/Eletroquimica-68-320.jpg)