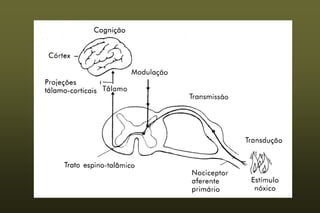
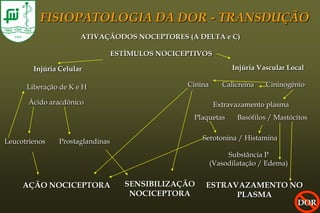
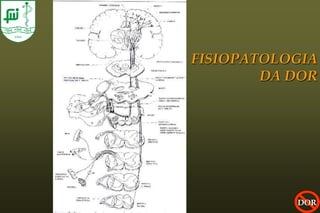
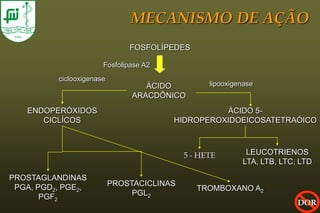
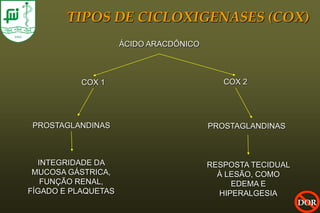
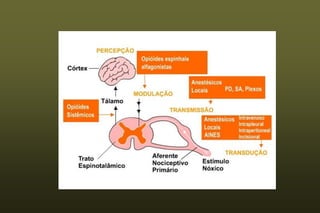
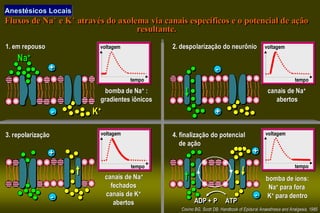
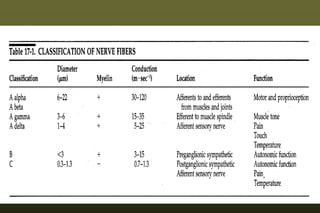
O documento discute conceitos sobre dor pós-operatória, incluindo dor nociceptiva, neuropática e mista. Também aborda a fisiopatologia da dor aguda e crônica, mecanismos de transdução, transmissão e modulação da dor, além de efeitos adversos fisiológicos da dor e opções farmacológicas para seu tratamento.