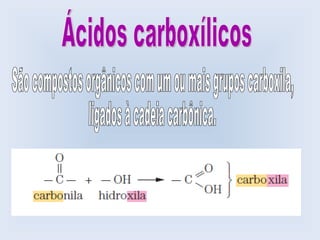
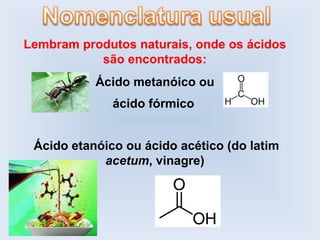
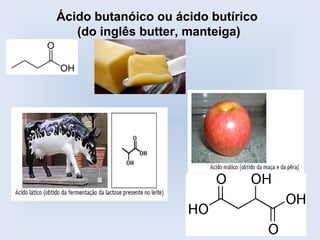
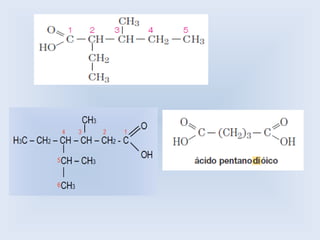
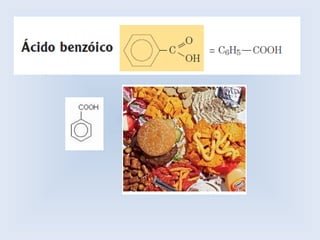
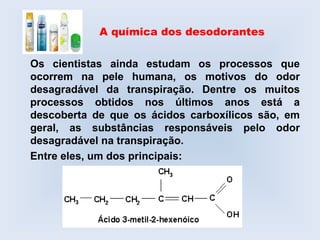
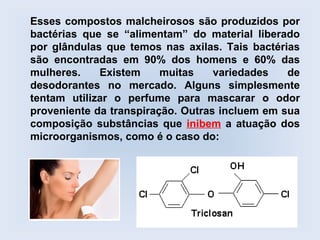
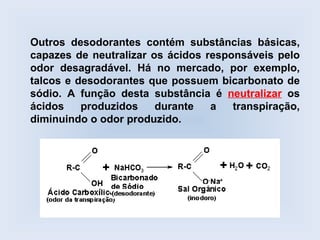
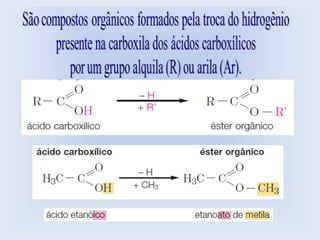
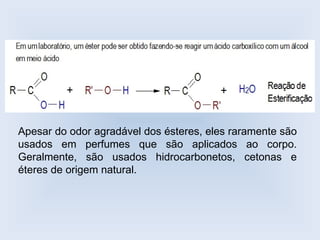
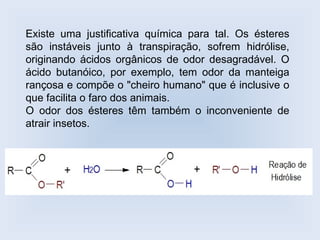
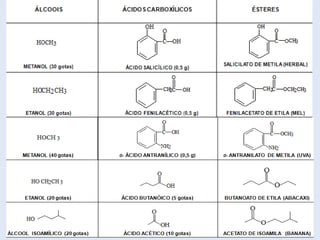
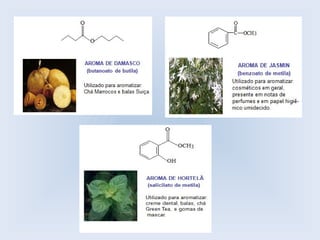
O documento descreve as principais características de ácidos orgânicos e ésteres. Define que ácidos carboxílicos são responsáveis pelo odor desagradável da transpiração e que desodorantes usam substâncias básicas para neutralizá-los. Também explica que ésteres são usados em aromatizantes de alimentos e produtos como ceras, óleos e gorduras.







![Diclofenaco:
2-[2-[(2,6-
dichlorophenyl)amino]phenyl]acetic
acid - ação sobretudo analgésica e
antiinflamatória,](https://image.slidesharecdn.com/acidoscarboxilicoseesteres-120627205324-phpapp01/85/Acidos-carboxilicos-e-esteres-27-320.jpg)
