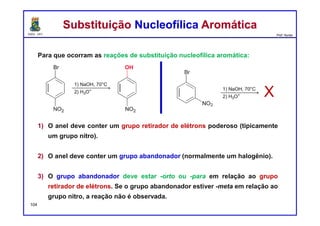
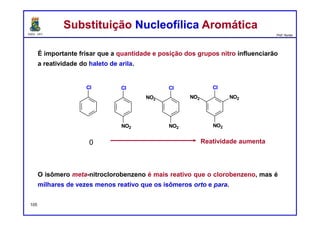
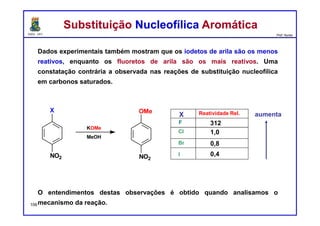
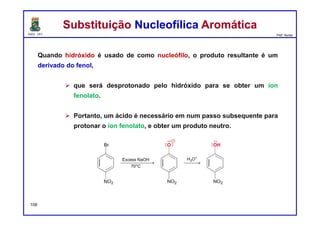
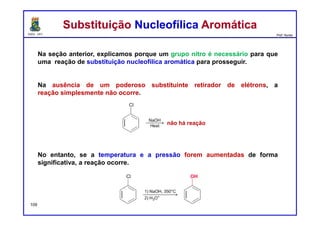
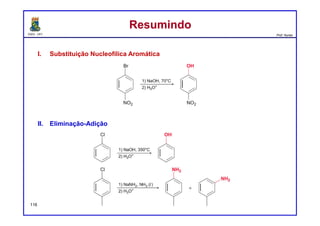
I. As reações de substituição nucleofílica aromática requerem a presença de um grupo retirador de elétrons (nitro) orto ou para em relação a um grupo abandonador (halogênio) no anel aromático.
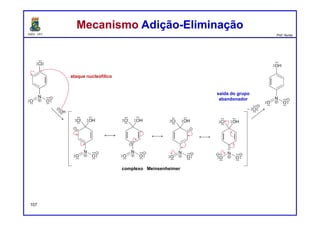
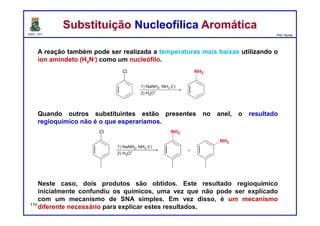
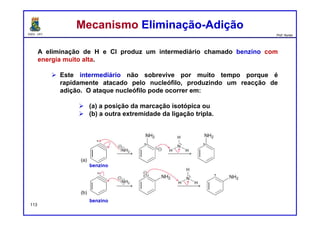
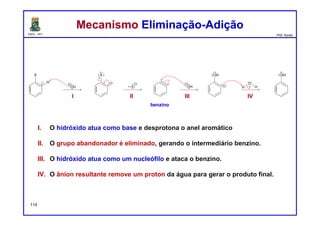
II. O mecanismo envolve a formação de um intermediário benzino que é atacado pelo nucleófilo, levando a dois possíveis produtos.
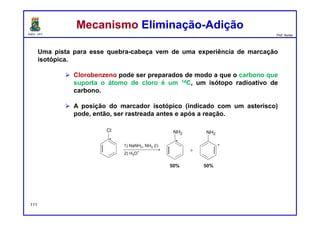
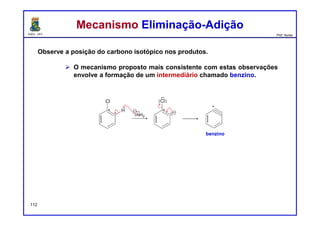
III. Experimentos de marcação isotópica confirmam o mecanismo de eliminação-adição.