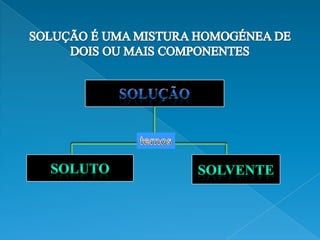
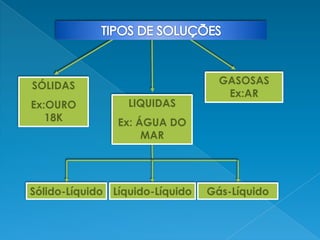
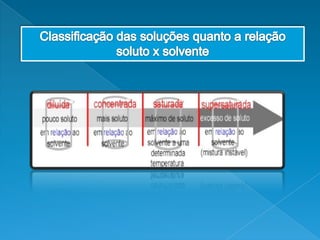
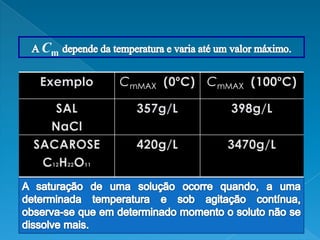
O documento discute soluções químicas, definindo-as como misturas homogêneas de dois ou mais componentes. Explica que o soluto é o componente em menor quantidade e o solvente é o componente que dissolve o soluto. Também classifica diferentes tipos de soluções e discute como a concentração de uma solução depende da quantidade relativa de soluto e solvente.