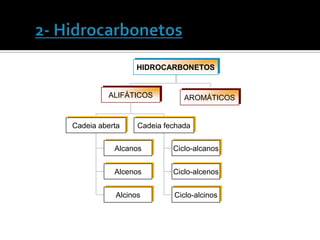
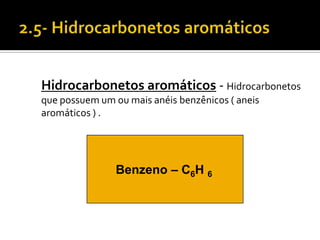
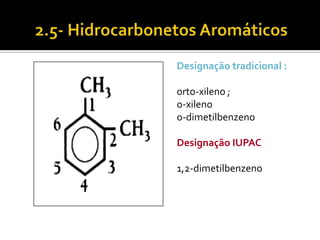
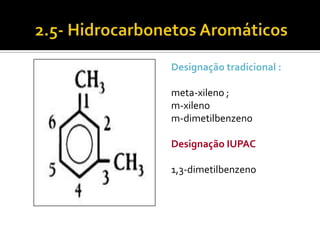
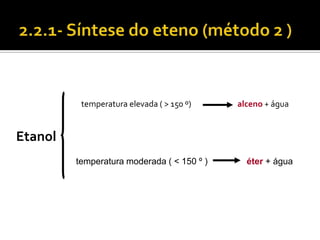
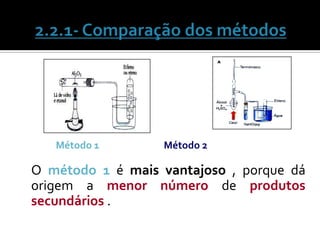
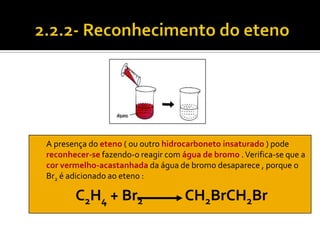
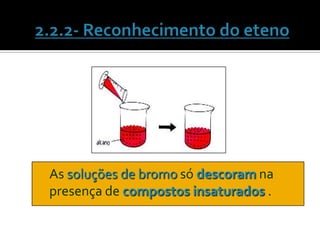
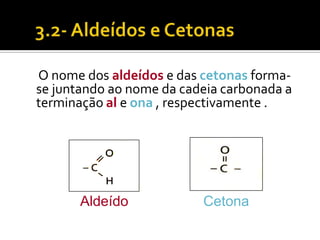
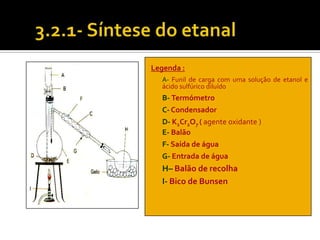
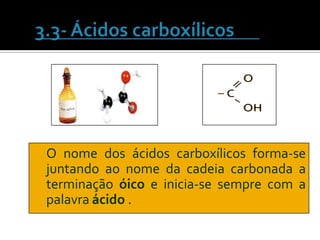
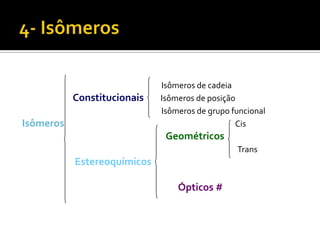
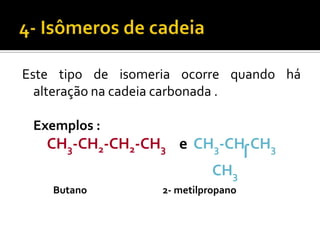
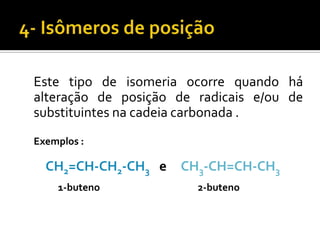
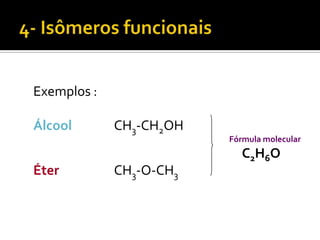
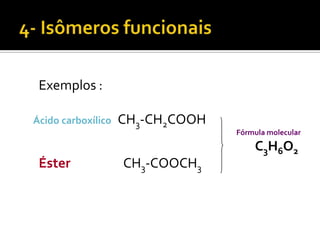
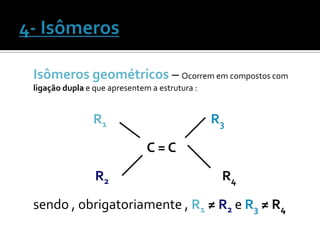
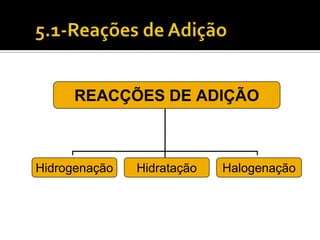
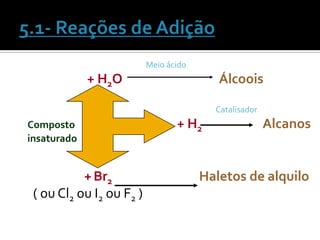
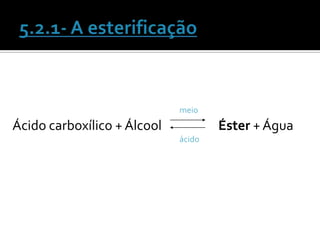
O documento discute vários tópicos da química orgânica, incluindo hidrocarbonetos, álcoois, aldeídos, cetonas, ácidos carboxílicos e ésteres. Ele fornece detalhes sobre a estrutura, nomenclatura e propriedades destes compostos, além de descrever métodos de síntese como a oxidação de álcoois e a esterificação. O documento também aborda isômeros e reações de compostos orgânicos.