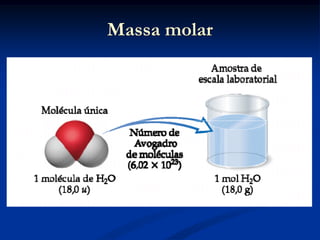
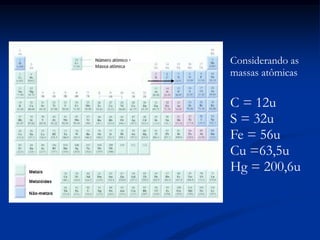
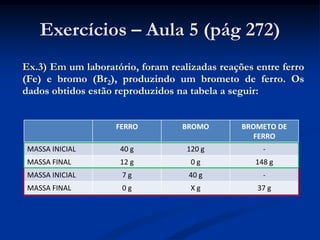
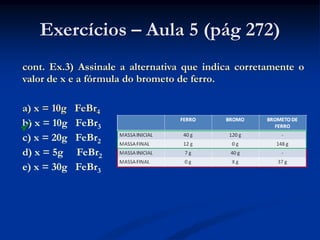
O documento apresenta os conceitos de massa atômica, massa molecular, número de Avogadro, mol e massa molar. Também aborda equações químicas e as leis das reações químicas de Lavoisier e Proust. Há exercícios sobre cálculos estequiométricos envolvendo essas grandezas.