1) O documento apresenta vários problemas de química envolvendo cálculos de concentrações de soluções e quantidades de substâncias.
2) São abordados temas como neutralização de antiácidos, riscos de exposição a gases como monóxido de carbono no ar, concentração ideal de oxigênio dissolvido em aquários, e quantidades máximas de compostos cancerígenos em ambientes.
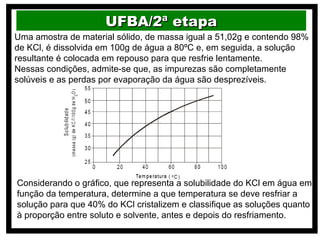
3) São também apresentados cálculos envolvendo tratamento de água potável, solubilidade de sais como cloreto de potá