O documento apresenta 15 questões de múltipla escolha sobre classificação da matéria e propriedades químicas de substâncias e misturas. As questões abordam temas como representação de compostos, ligas metálicas, propriedades da água, estados físicos de elementos químicos e reconhecimento de substâncias a partir de suas características.











![Gabarito:
Resposta da questão 1:
[E]
Resposta da questão 2:
[E]
Resposta da questão 3:
[A]
Resposta da questão 4:
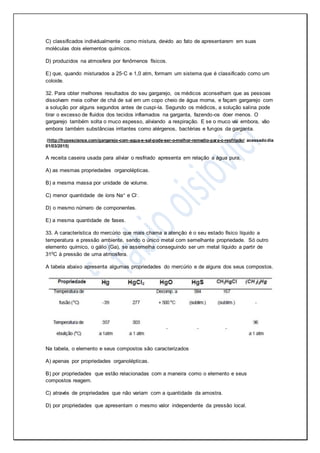
a) De acordo com a tabela, o ponto de fusão da substância contida no frasco é 23 C e o
ponto de ebulição é 77 C. Como 23 C (S L) 25 C 77 C (L G), concluímos que o
estado de agregação da substância é líquido.
b) A solubilidade da substância em água a 25 C é 0,1g 100 g de 2H O. Então:
0,1 g 2100 g (H O)
m g 2200,0 g (H O)
m 0,2 g (massa que se dissolveu de X)
Foram adicionados 56,0 g da substância X, logo 55,8 g (56,0 g 0,2 g) não dissolveu.
c) Como a 25 C a densidade da substância X é 3
1,59 g cm e este valor é maior do que a
densidade da água, que é de 3
1,00 g cm , conclui-se que X fica na parte inferior do recipiente.
Resposta da questão 5:
[A]
É correto afirmar que, em Encélado a existência do oceano líquido é uma hipótese possível,
pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida:
NaCl(s)
2 (l)H O
Na+(aq) + Cl-(aq)
Resposta da questão 6:
[B]
Resposta da questão 7:
[A]
Resposta da questão 8:
[E]
Resposta da questão 9:
[E]](https://image.slidesharecdn.com/listaprorclassmatria-170122213359/85/Classificacao-e-Propriedades-da-Materia-13-320.jpg)
![Resposta da questão 10:
[B]
Resposta da questão 11:
[B]
Resposta da questão 12:
[E]
Resposta da questão 13:
[C]
Resposta da questão 14:
[D]
Resposta da questão 15:
[D]
Resposta da questão 16:
[E]
Resposta da questão 17:
[E]
Resposta da questão 18:
[D]
Resposta da questão 19:
[B]
Resposta da questão 20:
[C]
Resposta da questão 21:
[A]
Resposta da questão 22:
[A]
Resposta da questão 23:
[A]
Resposta da questão 24:
[C]
Resposta da questão 25:
[C]
Resposta da questão 26:
[B]
Resposta da questão 27:
[E]
Resposta da questão 28:
[B ]](https://image.slidesharecdn.com/listaprorclassmatria-170122213359/85/Classificacao-e-Propriedades-da-Materia-14-320.jpg)
![Resposta da questão 29:
[ A]
Resposta da questão 30:
[ E]
Resposta da questão 31:
[ B]
Resposta da questão 32:
[ E]
Resposta da questão 33:
[C ]
Resposta da questão 34:
[ D]
Resposta da questão 35:
[D ]
Resposta da questão 36:
[E ]
Resposta da questão 37:
[ B]](https://image.slidesharecdn.com/listaprorclassmatria-170122213359/85/Classificacao-e-Propriedades-da-Materia-15-320.jpg)