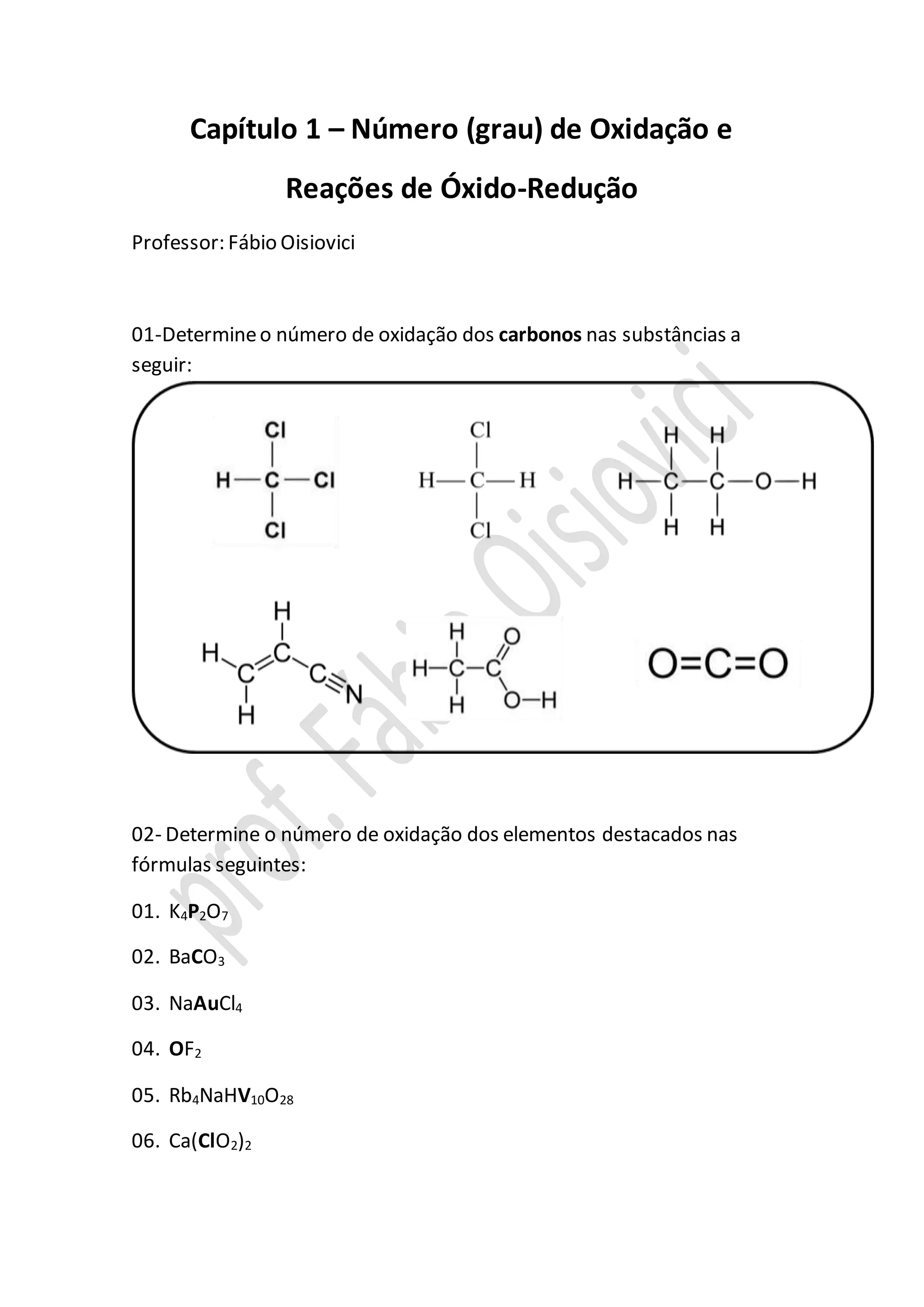
O documento discute conceitos de número de oxidação e reações de oxirredução. Apresenta 34 questões sobre determinação de número de oxidação de elementos em diferentes compostos químicos e identificação de agentes oxidantes e redutores em reações de oxirredução.