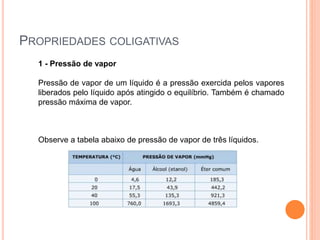
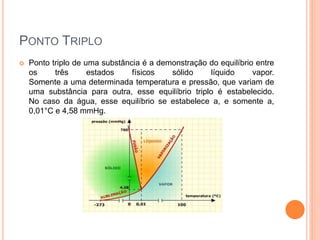
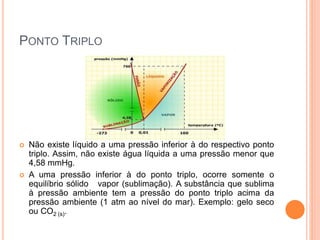
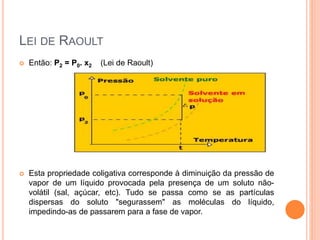
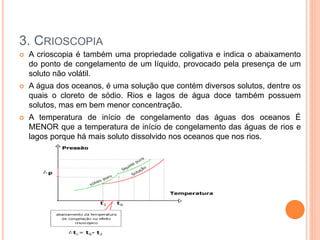
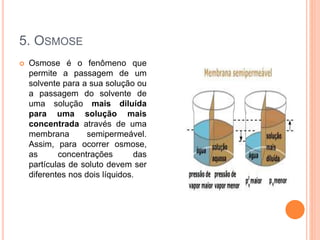
O documento discute propriedades coligativas como pressão de vapor, ponto de fusão, ponto de ebulição e osmose. Explica como a presença de um soluto afeta essas propriedades, incluindo a Lei de Raoult e como soluções afetam a temperatura de fusão e ebulição de um solvente. Também fornece exemplos como o sal abaixando o ponto de congelamento da água e aumentando o ponto de ebulição para cozinhar macarrão mais rápido.