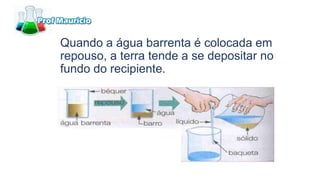
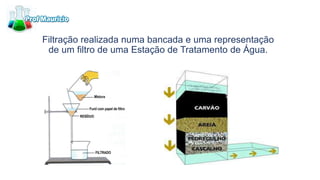
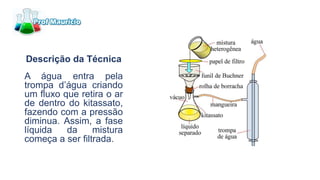
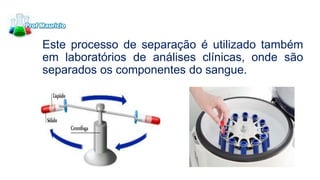
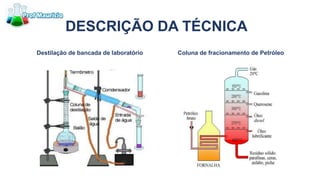
Este documento descreve 10 métodos de separação de misturas: 1) Decantação, 2) Funil de decantação, 3) Filtração simples, 4) Filtração a vácuo, 5) Centrifugação, 6) Destilação simples, 7) Destilação fracionada, 8) Dissolução fracionada, 9) Evaporação e 10) Separação magnética. Cada método explora diferenças nas propriedades físicas dos componentes da mistura para permitir sua separação.