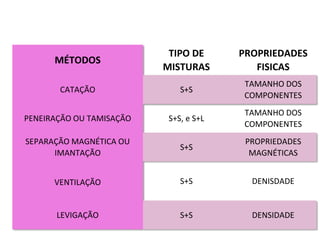
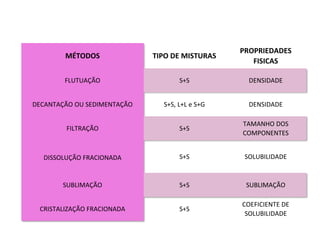
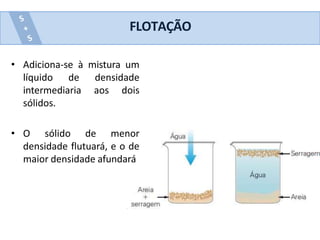
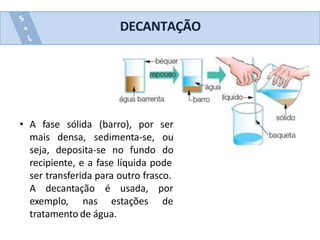
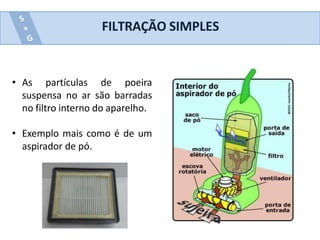
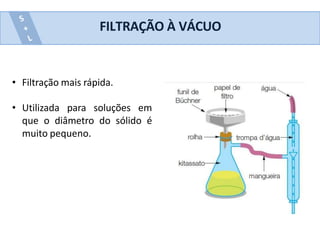
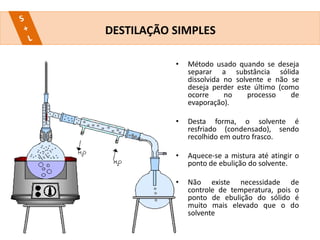
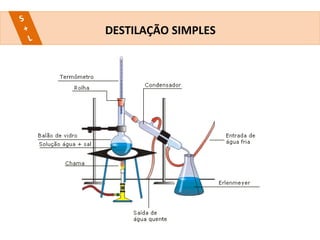
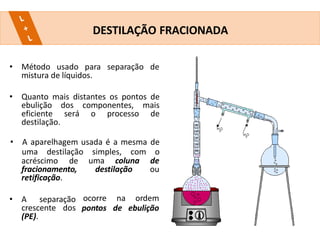
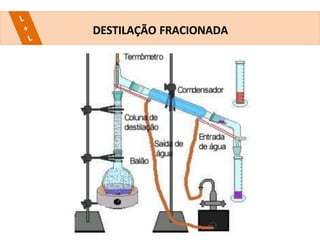
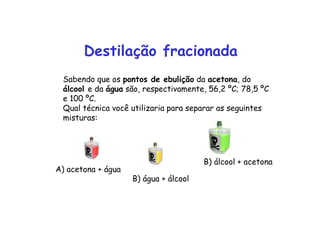
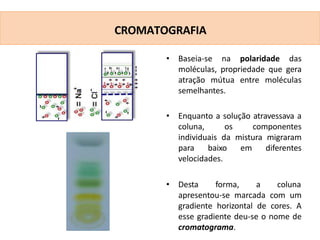
Este documento descreve vários métodos de separação de misturas heterogêneas e homogêneas, incluindo separação por propriedades físicas como tamanho de partículas, densidade e propriedades magnéticas. Alguns métodos comuns são catação, peneiração, separação magnética, decantação, filtração, flotação, dissolução fracionada e destilação.