Introdução à Reações Orgânicas
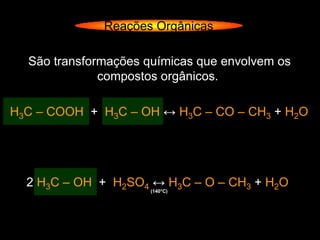
- 1. Reações Orgânicas São transformações químicas que envolvem os compostos orgânicos. H3C – COOH + H3C – OH ↔ H3C – CO – CH3 + H2O 2 H3C – OH + H2SO4 ↔ H3C – O – CH3 + H2O (140°C)
- 2. Reações Orgânicas São transformações químicas que envolvem os compostos orgânicos. Componentes Substrato é o composto orgânico principal que será transformado. Reagente é todo composto, orgânico ou inorgânico, que será utilizado para transformar o substrato.
- 3. Reações Orgânicas São transformações químicas que envolvem os compostos orgânicos. H3C – COOH + H3C – OH ↔ H3C – CO – CH3 + H2O Substrato Reagente Produtos da Reação 2 H3C – OH + H2SO4 ↔ H3C – O – CH3 + H2O (140°C) Substrato Reagente Produtos da Reação
- 4. Reações Orgânicas Tipos de Cisões ou Quebras de Ligações Homolítica ou Homólise É toda quebra de ligação entre elementos iguais (Eletronegatividades Iguais) A A A A A A Normalmente substâncias apolares sofrem cisão homolítica e formam radicais livres. H2 ( H H) Cl2 (Cl Cl)
- 5. Reações Orgânicas Tipos de Cisões ou Quebras de Ligações Homolítica ou Homólise É toda quebra de ligação entre elementos iguais (Eletronegatividades Iguais) A A A A A A Em condições especiais (presença de catalisador) substâncias apolares podem sofrer cisão heterolítica. Br2 Cl2 ( Br+ Br-) ( Cl+ Cl-) FeBr3 AlCl3
- 6. Reações Orgânicas Tipos de Cisões ou Quebras de Ligações Heterolítica ou Heterólise É toda quebra de ligação entre elementos diferentes (Eletronegatividades Diferentes) A B A B A+ B- Normalmente substâncias polares sofrem cisão heterolítica e formam íons. HCl ( H+ Cl-) HBr ( H+ Br-)
- 7. Reações Orgânicas Tipos de Cisões ou Quebras de Ligações Heterolítica ou Heterólise É toda quebra de ligação entre elementos diferentes (Eletronegatividades Diferentes) A B A B A+ B- Em condições especiais (Luz, Calor ou Peróxido) substâncias polares podem sofrer cisão homolítica. HBr HCl (H Br ) uv (H Cl ) Peróxido
- 8. Reações Orgânicas Tipos de Reagentes Eletrófilo ou Eletrofílico São os reagentes amigos de elétrons (Ácidos de Lewis) Cátions Cl+, NO2+, SO3H+... Cl Cl Sem Elétrons Livres Al Cl Carbocátions H3C+
- 9. Reações Orgânicas Tipos de Reagentes Nucleófilo ou Nucleofílico São os reagentes amigos de núcleos (Bases de Lewis) Ânions OH–, OR–, SR–... N Com Elétrons Livres H H H Carboânions H5C6-
- 10. Reações Orgânicas Tipos de Reagentes Radical Livre ou Radical São formados através uma homólise, onde cada parte da quebra permanece com o seu elétron de origem. H ; Cl ; Br ; H3C ; etc.
- 11. Reações Orgânicas Tipos de Intermediários Carbocátion ou Íon Carbônion São espécies formadas no meio da reação (provenientes do substrato) carregadas positivamente. H3C – CH – CH3 +
- 12. Reações Orgânicas Tipos de Intermediários Carboânion ou Íon Carbânion São espécies formadas no meio da reação (provenientes do substrato) carregadas negativamente. - Cl H3C – CH2 NH2
- 13. Reações Orgânicas Tipos de Intermediários Radical Livre ou Radical São espécies formadas no meio da reação (provenientes do substrato) através de uma cisão homolítica. H3C – CH2 – CH2
- 14. Reações Orgânicas Classificação das Reações Adição É toda reação onde há formação de um único produto. H2C = CH – CH3 + HCl H3C – CH – CH3 – + + – | Cl
- 15. Reações Orgânicas Classificação das Reações Substituição É toda reação onde há uma troca entre o substrato e o reagente. O O H3C–C–OH + H3C – OH H3C–C–O–CH3 + H2O + – – + H+
- 16. Reações Orgânicas Classificação das Reações Eliminação É toda reação onde há perda(s) do substrato e/ou do reagente. + – NaNH2 H3C – CH – CH2 + + – H3C – CH = CH2 + NaCl +NH3 | | – Cl + H
- 17. Reações Orgânicas Classificação das Reações Desidratação É toda reação onde o substrato perde água. H2SO4 H3C – CH – CH2 + H3C – CH = CH2 + H2O | | 180°C OH H
- 18. Reações Orgânicas Classificação das Reações Oxidação É toda reação onde o nox de uma espécie do substrato aumenta. CH3 COOH + KMnO4 + H2O H2SO4 3- 3+ nox ↑ oxidação
- 19. Reações Orgânicas Classificação das Reações Redução É toda reação onde o nox de uma espécie do substrato diminui. O OH || | H3C – C – CH3 + LiAlH4 H3C – CH – CH3 2+ 0 nox ↓ redução
- 20. Reações Orgânicas Classificação das Reações Polimerização É toda reação onde há formação de moléculas gigantescas através de moléculas menores. ∆ n H2C = CH2 – [H2C – CH2] – catalisadores n Monômero Polímero
