Hibridização Carbono
- 1. HIBRIDIZAÇÃO DO CARBONO (OU HIBRIDAÇÃO) Química Orgânica – 3º Ano Prof. Claudinei O. Oliveira
- 2. HIBRIDIZAÇÃO DO CARBONO Introdução Foi Kekulé, 1858, quem estabeleceu a tetravalência do elemento carbono.
- 3. Introdução Assim, a molécula de metano (CH4) costuma ser representada como: HIBRIDIZAÇÃO DO CARBONO H I H – C – H I H Fórmula estrutural plana do metano.
- 4. Introdução Com a descoberta de novos fenômenos químicos, como por exemplo isomeria óptica, houve necessidade de aperfeiçoar o modelo de molécula plana apresentado. HIBRIDIZAÇÃO DO CARBONO
- 5. Introdução Desse modo, Le Bel e Van’t Hoff, em 1874, lançaram a idéia do carbono tetraédrico, portanto espacial. HIBRIDIZAÇÃO DO CARBONO
- 11. O carbono no estado fundamental HIBRIDIZAÇÃO DO CARBONO
- 12. O carbono hibridizado HIBRIDIZAÇÃO DO CARBONO
- 13. Então, o que realmente acontece com o C? A hibridação é um fenômeno que permite ao átomo realizar um número maior de ligações, aumentando assim a sua estabilidade. Hibridação consiste na fusão de orbitais atômicos incompletos, que se transformam, originando novos orbitais, em igual número. Esses novos orbitais são denominados de orbitais híbridos. Existem 3 tipos de hibridações para o átomo de carbono: sp3, sp2 e sp
- 14. Hibridização sp3 Na hibridização sp3 um elétron “s” é promovido para o orbital “p” vazio, originando o carbono no estado ativado (intermediário).
- 15. Hibridização sp3 Em seguida, há “fusão” entre o orbital “s” e os três obtitais “p”. Daí, hibridização sp3. HIBRIDIZAÇÃO DO CARBONO
- 16. Hibridização sp3 Carbono hibridizado (gráfico energético) HIBRIDIZAÇÃO DO CARBONO
- 17. Hibridização sp3 Carbono hibridizado (formas dos orbitais híbridos) HIBRIDIZAÇÃO DO CARBONO
- 18. Hibridização sp3 Nas ligações com outros átomos, forma quatro ligações “sigma”. Hibridação na molécula do metano CH4 Geometria tetraédrica
- 19. Hibridização sp2 Na hibridização sp2 um elétron “s” é também promovido para o orbital “p” vazio, originando o carbono no estado ativado (intermediário). Entretanto, a “fusão” de orbitais ocorre entre o orbital “s” e dois “p”.Daí, hibridização sp2. Note que um dos orbitais “p” permaneceu puro.
- 20. Hibridização sp2 Carbono hibridizado (formas dos orbitais híbridos)
- 21. Hibridização sp2 Nas ligações com outros átomos, forma três ligações “sigma” e uma “pi”. Geometria trigonal planar
- 22. Hibridização sp2 Carbono hibridizado (na molécula de eteno) HIBRIDIZAÇÃO DO CARBONO
- 23. Hibridização sp De forma semelhante, na hibridização sp um elétron “s” é também promovido para o orbital “p” vazio, originando o carbono no estado ativado (intermediário). Agora, a “fusão” de orbitais ocorre entre o orbital “s” e um “p”, permanecendo dois orbitais “p” puros. Daí, hibridização sp.
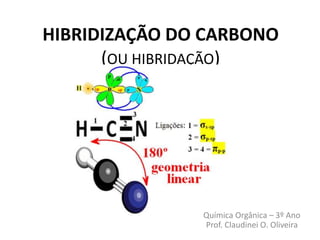
- 24. Hibridização sp Nas ligações com outros átomos, forma duas ligações “sigma” e duas “pi”. Geometria linear Ângulo de 180
- 25. Hibridização sp Carbono hibridizado (a molécula de etino) HIBRIDIZAÇÃO DO CARBONO
- 28. Encerrando . . . Salientamos que o fenômeno da hibridização não é exclusividade do elemento carbono. HIBRIDIZAÇÃO DO CARBONO
- 29. Encerrando . . . O enxofre, por exemplo, na formação do composto SF6 também apresenta o fenômeno da hibridização. HIBRIDIZAÇÃO DO CARBONO
