O documento discute geometria e isomeria em compostos de coordenação. Ele define números de coordenação e descreve fatores que afetam a geometria de complexos com diferentes números de coordenação. Além disso, o documento explica vários tipos de isomeria que podem ocorrer em compostos de coordenação, incluindo isomeria de ligação, isomeria de ionização, isomeria de hidratação e isomeria geométrica e óptica em complexos octaédricos.

![COMPOSTOS DE COORDENAÇÃO:
• Definições Importantes:
– Número de Coordenação:
• Quantidade de ligantes coordenados ao metal ou íon
metálico na esfera de coordenação.
• Podem variar de algumas poucas unidades até 12.
• Em algumas situações o número de coordenação não é
evidente pela composição do sólido. Exemplo:
– DRX do CoCl2.6H2O identifica o complexo neutro
[Co(Cl)2(OH2)4] e duas moléculas de água não coordenadas que
ocupam posições bem definidas no cristal (água de
cristalização).
Março/2010 2Prof. Dr.Ary Maia](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-2-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
– Complexo de Esfera Interna x Complexo de Esfera
Externa :
• Cátions complexos podem se associar eletrostaticamente
a ligantes aniônicos (e por interações fracas às moléculas
do solvente), sem deslocar os ligantes já presentes.
• Exemplo:
Março/2010 3Prof. Dr.Ary Maia
[Mn(OH2)6]2+ e SO4
2-
{[Mn(OH2)6]2+SO4
2-} [Mn(OH2)5 SO4]
A concentração no equilíbrio do complexo de esfera externa pode,
dependendo da concentração, exceder a do complexo de esfera interna.
Complexo de Esfera Externa Complexo de Esfera Interna](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-3-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
– Fatores que afetam o Número de Coordenação:
• Tamanho do átomo ou íon central:
– Raios maiores favorecem números de coordenação maiores.
– Elementos situados à esquerda de um período apresentam íons maiores (Logo
NC maiores).
• Interações espaciais entre os ligantes:
– Ligantes volumosos resultam em números de coordenação menores, ainda mais
se forem carregados.
• Interações eletrônicas entre o átomo ou o íon central e os
ligantes:
– Elementos situados à esquerda de um período apresentam poucos elétrons na
sua configuração o que significa poder receber mais elétrons das bases de
Lewis. Ex. [Mo(CN)8]4-.
– Ligantes que podem formar ligações múltiplas com o átomo ou íon central
tendem a gerar NC menores (Ex. MnO4
- e CrO4
-).
Março/2010 4Prof. Dr.Ary Maia](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-4-320.jpg)



![COMPOSTOS DE COORDENAÇÃO:
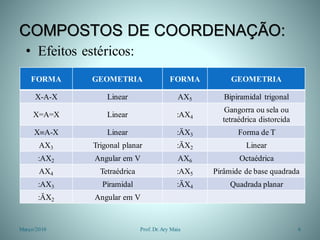
• Constituição e Geometria:
– Números de Coordenação Baixos:
• Compostos bicoordenados Cu+1,Ag+1 , Au+1 , Hg+2.
• Adquirem ligantes adicionais (quando em excesso) para formação de
complexos tri e tetracoordenados.
• Exemplos: [AgCl2]-1, [HgMe2], CuCN (polímero de cadeia linear,
com NC=2 -Cu-CN-Cu-CN-).
– NC = 4:
• Podem apresentar geometria tetraédrica ou quadrada planar.
• Para átomo ou íon central pequeno ou ligantes grandes há
favorecimento de complexos tetraédricos.
• Exemplos: [BF4]-, [Ni(CO)4], [Zn(NH3)4]2+
• Configurações eletrônicas d8 e s1d7 induzem a geometria quadrada
planar.
• Exemplos: [Pt(NH3)4]2+, [PdCl4]2-, [Ir(CO)Cl(PΦ3)2]
Março/2010 9Prof. Dr.Ary Maia](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-9-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
• Constituição e Geometria:
– NC=5:
• Complexos com geometria limite entre piramidal quadrática e
bipiramidal trigonal.
• Pouca diferença de energia entre as formas.
• O [Ni(CN)5]3- pode se apresentar na duas
formas.
• Em solução, com ligante monodentados, estes
complexos são altamente fluxionais (contercer
em diferentes formas) Pseudo-rotação de
Berry.
Março/2010 10Prof. Dr.Ary Maia
Química Inorgânica – Shriver, D. , Atkins, P. et al. – 4ª Ed. – Porto Alegre (2008)](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-10-320.jpg)

![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA:
– Fórmula Molecular não é suficiente para identificar um
composto, sem ambiguidade – Há isomeria:
• Isomeria de Ligação:
– Um ligante pode se ligar através de
diferentes átomos.
– Ex.: [Co(NO2)(NH3)5]2+ Isômero vermelho
(ligação nitrito) e isômero amarelo (ligação
nitro).
Química Inorgânica – Shriver, D. , Atkins, P. et al. – 4ª
Ed. – Porto Alegre (2008)
• Isomeria de Ionização:
– Um ligante e um contra-íon trocam de lugar em um composto.
– Ex.: [Pt(NH3)4Cl2]Br2 e [Pt(NH3)4Br2]Cl2
– Se os sais complexos são solúveis a diferenciação pode se fazer através da
identificação do íon livre em solução (Br- ou Cl- no exemplo anterior).
Março/2010 12Prof. Dr.Ary Maia](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-12-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA (cont.):
• Isomeria de Hidratação:
– Parecido com Isomeria de Ionização, mas ocorre quando um dos ligantes é a água.
– Ex.: Composto com fórmula molecular CrCl3.6H2O – 3 isômeros diferentes:
» [Cr(H2O)6]Cl3 VIOLETA
» [Cr(H2O)5Cl]Cl2.H2O VERDE PÁLIDO
» [Cr(H2O)4Cl2]Cl.2H2O VERDE ESCURO
• Isomeria de Coordenação:
– Íons complexos diferentes a partir de uma mesma fórmula molecular.
– Ex.: A fórmula molecular Cr(CN)3.Co(CN)3.6NH3 pode representar os complexos:
» [Co(NH3)6][Cr(CN)6] ou [Cr(NH3)6][Co(CN)6]
– Em um primeiro momento é necessário definir-se quais ligantes se
ligam com quais metais e através de quais átomos doadores
(ISOMERIA ESTRUTURAL), para então considerar-se as diversas
possibilidades de arranjos tridimensionais, que podem resultar em
isomeria geométrica e isomeria ótica (ESTEREOISOMERIA).
Março/2010 13Prof. Dr.Ary Maia](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-13-320.jpg)


![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA (cont.):
– Complexos Octaédricos:
• Isomeria Geométrica:
– [MA6] e [MA5B]: Não apresentam isômeros.
– [MA4B2]: Isômeros cis e trans:
– [MA3B3]: Isômeros mer (meridianal) e fac (facial):
Março/2010 16Prof. Dr.Ary Maia
Química Inorgânica –
Shriver, D. , Atkins, P.
et al. – 4ª Ed. – Porto
Alegre (2008)
Química Inorgânica –
Shriver, D. , Atkins, P.
et al. – 4ª Ed. – Porto
Alegre (2008)](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-16-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA (cont.):
– Complexos Octaédricos:
• Isomeria Geométrica:
– [MA2B2C2]: 5 isômeros geométricos diferentes
» Um com todos os ligantes trans (57).
» Três com um par trans e os outros dois cis (58,59,60).
» Um (enanciomérico) com todos os ligantes cis (61).
Março/2010 17Prof. Dr.Ary Maia
Química Inorgânica – Shriver, D. , Atkins, P. et al. – 4ª Ed. – Porto Alegre (2008)](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-17-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA (cont.):
– Complexos Octaédricos:
• Isomeria Ótica:
– Várias possibilidades de arranjo para isomeria ótica, independente de ligantes mono
ou polidentados.
– Complexos do tipo [MA2B2C2]:
– Complexos do tipo [Mn(acac)3]:
Março/2010 18Prof. Dr.Ary Maia
Química Inorgânica –
Shriver, D. , Atkins, P.
et al. – 4ª Ed. – Porto
Alegre (2008)
Química Inorgânica –
Shriver, D. , Atkins, P.
et al. – 4ª Ed. – Porto
Alegre (2008)](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-18-320.jpg)
![COMPOSTOS DE COORDENAÇÃO:
• ISOMERIA (cont.):
– Complexos Octaédricos:
• Isomeria Ótica:
– Complexos do tipo [CoCl2(en)2]+:
» Produto da reação do cloreto de cobalto (III) com a etilenodiamina, na razão
molarde 1:2.
» Produto 66 (íon cis-diclorobis(etilenodiaminocobalto (III)) é violeta o
produto 67 (íon trans-diclorobis(etilenodiaminocobalto (III)) é verde.
Março/2010 19Prof. Dr.Ary Maia
Química Inorgânica –
Shriver, D. , Atkins, P.
et al. – 4ª Ed. – Porto
Alegre (2008)](https://image.slidesharecdn.com/geometriadecomplexos-161008182713/85/Geometria-de-complexos-19-320.jpg)

