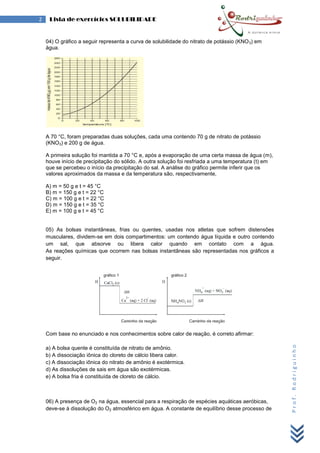
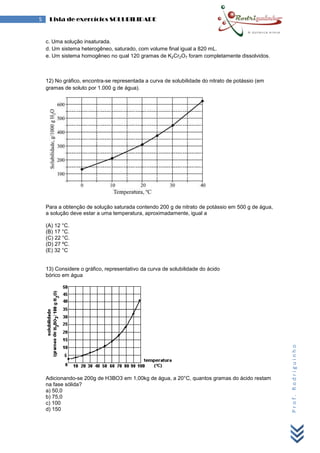
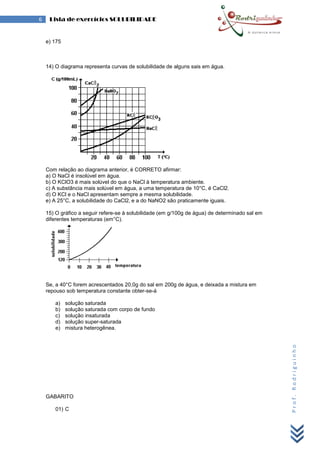
O documento apresenta 15 questões sobre solubilidade de sais em água em diferentes temperaturas. As questões abordam conceitos como curvas de solubilidade, soluções saturadas, supersaturadas e sistemas heterogêneos. O gabarito fornecido responde corretamente às 15 questões.